
ijͬѧͨ������װ�òⶨM ��Ʒ��ֻ��Fe��Al��Cu���и��ɷֵ�����������ȡ������ ����Ϊm g ��M ��Ʒ����ʵ��1����ͼ1����ʵ��2����ͼ2������ʵ�飬��ͬѧ˳�������ʵ�鲢�����������ֱ�ΪV1 mL ��V2 mL(�����㵽��״����)��
����Ϊm g ��M ��Ʒ����ʵ��1����ͼ1����ʵ��2����ͼ2������ʵ�飬��ͬѧ˳�������ʵ�鲢�����������ֱ�ΪV1 mL ��V2 mL(�����㵽��״����)��
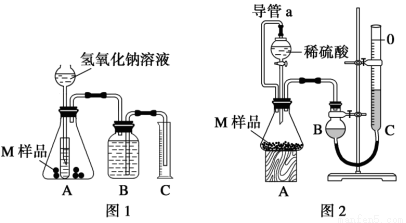
��1��ʵ��1 װ����С�Թܵ�������_______________��
��2������ʵ��2��ƽ�Ӷ���ǰӦ���ν��е����ֲ����ǣ�
��______________����________________________��
��3��ʵ��1 ����ʵ��ǰ��B ƿ��ˮû��װ����ʹ����������_____ (�ƫ����ƫС������Ӱ�족����ͬ)������ȥʵ��2 �е���a��ʹ����������_____________��
��4����ʵ����Ҫ0.50 mol��L��1 ��NaOH ��Һ470 mL����ش���������
������ʱӦ����______g NaOH�����ƹ�����������____________ (����������)��
������NaOH ��Һʱ��NaOH �����к���Na2O ���ʻᵼ��������ҺŨ��________��(�ƫ����ƫС������Ӱ�족)��
��5����ʵ��������ϡ��������98%��Ũ���ᣨ�� =1.84g/cm3�����Ƶģ�������Ũ�������������ˮ��ϣ���������Һ���������ʵ���Ũ��_________9.2mol/L���������=��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ׯ�Ӹ��и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪N2��g��+3H2��g�� 2NH3��g����H=��92.4kJ•mo1��1�����н�����ȷ���ǣ� ��
2NH3��g����H=��92.4kJ•mo1��1�����н�����ȷ���ǣ� ��
A�� ���ܱ������м���1mol N2��3mol H2��ַ�Ӧ����92.4kJ
B�� N2��g��+3H2��g�� 2NH3��l����H=��QkJ•mo1��1����Q��92.4
2NH3��l����H=��QkJ•mo1��1����Q��92.4
C�� ����ѹǿ��ƽ�������ƶ���ƽ�ⳣ������
D�� ��һ�������·�Ӧ�ﵽƽ�⣬N2��ת����Ϊ20%����H2��ת����Ϊ60%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��ԭ�и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��1�����б�ʾ��ʹ���¶ȵ�������________��
��2�����в����У�����ƿ�����߱��Ĺ�����________(�����)��
A������һ�����ȷŨ�ȵı���Һ
B��������Һ
C����������ƿ������µ������������Һ
D��ȷϡ��ijһŨ�ȵ���Һ
E����ȡһ�������Һ��
F�����������ܽ��������
��3����ͼ��ijЩ�����Ŀ̶Ȳ���ʾ��ͼ��ͼ�и���������Ϊ��ʾ����������Ϊ��Ͳ����________(���ţ���ͬ)������Ϊ________mL��Ϊ�ζ��ܵ���________������Ϊ________mL��
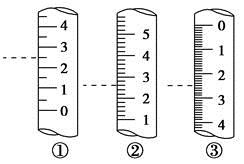
��4�����п������ڴ��������ʹ���õ����ݱ���ȷ����ƫС����________��
A����ȡ4.2 g NaCl����ʱ��������������̣� NaCl�����������
B��ʹ������ƿ������Һʱ������ҡ�Ⱥ�Һ����ڿ̶���
C����ʽ�ζ���������ˮϴ�Ӻ�ֱ�ӵ����Һ
D������Ͳ��ȡһ�������Һ��ʱ������Һ�����õĶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��ԭ�и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ����( )
A��FeBr2��Һ��ͨ��������Cl2��2Fe2����Cl2===2Fe3����2Cl��
B��Ca(HCO3)2��Һ�����NaOH��Һ��Ӧ��HCO��Ca2����OH��===CaCO3����H2O
C�������ʵ�����MgCl2��Ba(OH)2��HCl��Һ��ϣ�Mg2����2OH��===Mg(OH)2��
D��ͭ����ϡ�����У�Cu��4H����2NO===Cu2����2NO2����2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��ԭ�и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���в�����ȷ����( )

A��ֻ�Т� B���ڢ� C���ۢ� D��ȫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������������ѧ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA ��ʾ�����ӵ�������ֵ������������ȷ����( )
A����������ֽ��Ƶñ�״����1.12 L O2��ת�Ƶ�����ĿΪ 0.2 NA
B ������ͭ�뺬����4 mol ��Ũ���ᷴӦ�����ɵ����������е��Ļ��ϼ�Ϊ+4 ��
������ͭ�뺬����4 mol ��Ũ���ᷴӦ�����ɵ����������е��Ļ��ϼ�Ϊ+4 ��
C��1 mol ͭ������Ũ���ᷴӦ�����ɱ�����������Ϊ44.8 L
D��һ���¶��£�1 L 0.50 mol��L��1 NH4NO3 ��Һ�к���ԭ�Ӹ���ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������������ѧ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���ǣ� ��
A����25mL ��ˮ�еμ�5-6 �α���FeCl3 ��Һ����0.1molFeCl3�������� ��������С��NA
����������NA
B�������ЧӦ�ǽ�����������Һ�ı�������
C�����ὺ����ɱ���������Һ�м������ϡ�����Ƶ�
D���������������Ӿʱ������ɫ���֤�������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʦ���и߶�����ĩ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ�������·�����Ӧ3A(g)��2B(g) zC(g)��2D(g)����2L���ܱ������а�4 mol A��2 mol B��ϣ�2 min��Ӧ�ﵽƽ��ʱ����1.6 mol C���ֲ�÷�Ӧ����v(D)��0.2 mol��L�C1 ��min�C1 ��������˵������ȷ����( )
zC(g)��2D(g)����2L���ܱ������а�4 mol A��2 mol B��ϣ�2 min��Ӧ�ﵽƽ��ʱ����1.6 mol C���ֲ�÷�Ӧ����v(D)��0.2 mol��L�C1 ��min�C1 ��������˵������ȷ����( )
A��z��4
B��B��ת������40%
C��A��ƽ��Ũ����1.4 mol��L�C1
D��ƽ��ʱ����ѹǿ��ԭ����1. 2��
2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ������һ�и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ������������������ͻ���۶���ȷ����
ѡ�� | ʵ����� | ���������� | ���ͻ���� |
A | ������������Һ�У���μ��������ữ�����ᱵ��Һ | ������ɫ���� | �����������ᱵ�����ܽ���ˮ�ij��� |
B | ��SO2ͨ��������Ը��������Һ�� | ��Һ�Ϻ�ɫ��ȥ | SO2����Ư���� |
C | ������ͭƬ���������� | ��������ɫ���� | ������ͭ��������Һ��Ӧһ������NO2 |
D | ��ij��Һ�м���NaHCO3 | ������ɫ���� | ����Һ����ԭ�������������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com