
【题目】在一容积为2L的密闭容器内加入0.2mol的N2和0.6 mol的H2.在一定条件下发生如下反应:
N2(g)+3H2(g) ![]() 2NH3(g) △H<0反应中NH3的物质的量浓度的变化情况如图所示:
2NH3(g) △H<0反应中NH3的物质的量浓度的变化情况如图所示:

(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)=____mol/(L·min)
(2)反应达到平衡后,第5分钟末,保持其他条件不变,若改变反应温度,则NH3的物质的量浓度不可能为_________(填字母序号)。
A.0 20 mol/L B.0.1 mol/L C.0.10 mol/L D.0.08 mol/L
(3)反应达到平衡后,第5分钟末,保持其他条件不变,若只把容器的体积缩小一半,平衡_______移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数_________(填“增大”、“减小”或“不变”).
(4)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(设此时NH3的浓度为0.25mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。______
【答案】 0.025 AC 向正反应方向 不变 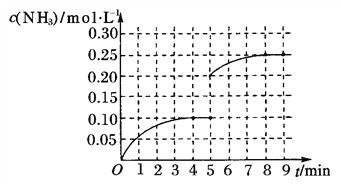
【解析】(1)结合图象可知,4min~5min时,氨气的物质的量浓度为0.1mol/L,氨气的浓度不再变化,说明正逆反应速率相等,此时已经达到平衡状态;平衡时氨气的浓度为0.1mol/L,时间为4min,则0~4min氨气的平均反应速率υ(NH3)=:v(NH3)= ![]() =0.025 mol/(Lmin),故答案为:0.025 mol/(Lmin);
=0.025 mol/(Lmin),故答案为:0.025 mol/(Lmin);
(2)改变反应温度,平衡一定移动,而氮气和氢气不可能完全转化为氨气,所以v(NH3)<0.20mol/L。A.如果氨气的浓度是0.20mol/L,则氮气与氢气完全转化,故错误;B.降低温度,氨气的浓度可能为0.12mol/L,故正确;C.温度改变,平衡一定移动,所以不可能为0.10mol/L,故错误;D.升高温度,平衡逆向移动,所以氨气浓度变小,可能为:0.08mol/L,故正确;故答案为:AC;
(3)该反应是气体体积减小的反应,把容器的体积缩小一半,增大了反应体系的压强,增大压强,平衡向气体体积减小的方向移动,即向正反应方向移动;化学平衡常数只与温度有关,温度不变,平衡常数不变,故答案为:向正反应方向;不变;
(4)把容器的体积缩小一半的瞬间氨气的浓度,氨气的浓度变为0.20mol/L,平衡后浓度约为0.25mol/L,所以第5分钟末到平衡时NH3浓度的变化曲线为: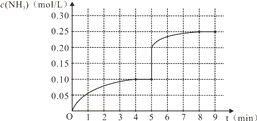 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】正常生活的细胞内时刻进行着复杂有序的新陈代谢活动,而新陈代谢同两种物质密切相关,即酶和ATP,下列关于二者的叙述正确的是( )
A. 酶是活细胞产生的只能在活细胞中起作用的有机物
B. ATP水解掉两个磷酸余下部分可成为RNA的组成单位
C. ATP中的A为腺嘌呤
D. 酶能催化化学反应是因为酶能够为化学反应提供能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由A、B、C、D四种金属按下表中装置图进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_______________。
(2)装置乙中正极的电极反应式是_______________。
(3)装置丙中溶液的pH________(填“变大”“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应中的能量变化,表述正确的是:
A. 氧化反应均为吸热反应
B. 断开化学键的过程会放出能量
C. 加热才能发生的反应一定是吸热反应
D. 放热反应中,反应物的总能量大于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生物体内有机化合物及其功能的叙述,不正确的是( )
A. 葡萄糖是细胞内主要的能源物质 B. 胰岛素能促进肝糖原分解
C. 脱氧核苷酸是DNA的基本组成单位 D. 纤维素是组成植物细胞壁的成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1mol的硫蒸汽和硫固体分别完全燃烧,前者△H比后者小
B. 在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热
C. 由C(s,石墨)═C(s,金刚石);△H=+1.9kJmol-1 可知,金刚石比石墨稳定
D. 反应热就是反应中放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
请回答该实验中的问题.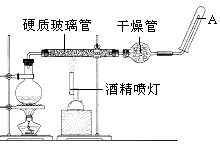
(1)写出该反应的反应方程式:
(2)如何检验该装置的气密性
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 .
(4)酒精灯和酒精喷灯点燃的顺序是 , 为什么
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 发酵粉中主要含有氢氧化钠,能使焙制出的糕点疏松多孔
B. 碘盐中的碘可以直接用淀粉检验
C. 硫酸氢钠属于盐类,其水溶液显中性
D. 碳酸氢钠可以用于治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.100 mol·L-1的NaOH溶液分别逐滴加入到20.00 mL 0.100 0 mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确的是( )
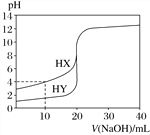
A. V(NaOH)=10.00 mL时,两份溶液中c(X-)>c(Y-)
B. V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
C. V(NaOH)=20.00 mL时,c(OH-)>c(H+)>c(Na+)>c(X-)
D. pH=7时,两份溶液中c(X-)=c(Na+)=c(Y-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com