
| 选项 | A | B | C | D |
| 强电解质 | KNO3 | H2SO4 | BaSO4 | HClO4 |
| 弱电解质 | HF | CaCO3 | HClO | CH3COONH4 |
| 非电解质 | SO2 | 金属Al | H2O | C2H5OH |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| 水 |
| 酒化酶 |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
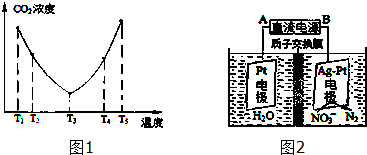
查看答案和解析>>
科目:高中化学 来源: 题型:
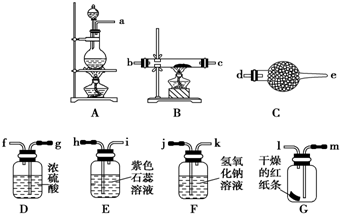
查看答案和解析>>
科目:高中化学 来源: 题型:
| 问题与猜想 | 实验步骤 | 实验现象 | 实验结论 |
| 问题2:小纸袋中的物质能否继续作干燥剂? | 取足量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁 | 不能继续作干燥剂 | |
| 问题3:甲猜想变质后的物质可能含有碳酸钙,该如何验证甲的猜想? | 该干燥剂样品中含有碳酸钙 |
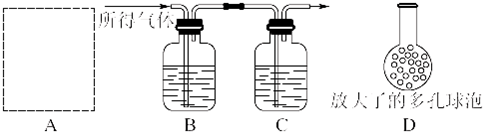
查看答案和解析>>
科目:高中化学 来源: 题型:
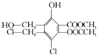 ,下列有关该物质的叙述正确的是( )
,下列有关该物质的叙述正确的是( )| A、1mol该物质最多可以消耗3 mol Na |
| B、1mol该物质最多可以消耗7 mol NaOH |
| C、不能与Na2CO3溶液反应 |
| D、易溶于水,可以发生加成反应和取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2个-CH3,能生成6种一氯代物 |
| B、3个-CH3,能生成4种一氯代物 |
| C、2个-CH3,能生成5种一氯代物 |
| D、4个-CH3,能生成4种一氯代物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com