
【题目】2mol A与2mol B混合于2L的密闭容器中反应:2A(g)+3B(g)2C(g)+zD(g)若2s后,A的转化率为50%,测得v(D)=0.25molL﹣1s﹣1 , 下列推断正确的是( )
A.v(C)=0.2 molL﹣1s﹣1
B.z=3
C.B的转化率为25%
D.C的体积分数为28.6%
【答案】D
【解析】解:若2s后,A的转化率为50%,则A转化的物质的量为2mol×50%=1mol,则
2A(g) | + | 3B(g) | 2C(g) | + | zD(g) | ||
开始 | 2 | 2 | 0 | 0 | |||
转化 | 1 | 1.5 | 1 | 0.5z | |||
2s后 | 1 | 0.5 | 1 | 0.5z |
v(D)=0.25molL﹣1s﹣1 , 即 ![]() =0.25molL﹣1s﹣1 , 解得z=2,
=0.25molL﹣1s﹣1 , 解得z=2,
A.化学反应速率之比等于化学计量数之比,v(C)=v(D)=0.25molL﹣1s﹣1 , 故A错误;
B.由上述计算可知,z=2,故B错误;
C.B的转化率为 ![]() ×100%=75%,故C错误;
×100%=75%,故C错误;
D.C的体积分数为 ![]() ×100%=28.6%,故D正确;
×100%=28.6%,故D正确;
故选D.
【考点精析】解答此题的关键在于理解化学平衡的计算的相关知识,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


科目:高中化学 来源: 题型:
【题目】现有下列物质:①NaCO310H2O晶体 ②铜 ③硫酸溶液 ④CO2 ⑤NaHSO4固体 ⑥Ba(OH)2固体 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3固体。
(1)上述物质属于电解质的有(填编号)。
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,写出该离子反应对应的化学方程式。
(3)制取⑦的化学方程式;将⑥的溶液滴加到⑤的溶液中至恰好完全沉淀时的离子方程式。
(4)17.1g⑩溶于水配成250mL溶液,SO42-的物质的量浓度为。
(5)②与⑨发生反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O当有0.6mol电子转移时,生成的气体标准状况下的体积为L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸在不同的反应中,可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,有关判断正确的是( )
①Zn+2HCl ![]() ZnCl2+H2↑;②NaOH+HCl
ZnCl2+H2↑;②NaOH+HCl ![]() NaCl+H2O;
NaCl+H2O;
③2HCl ![]() H2↑+Cl2↑
H2↑+Cl2↑
选项 | 有关判断 |
A | 反应①是置换反应,HCl表现还原性 |
B | 反应②是复分解反应,HCl表现氧化性 |
C | 反应③中HCl既表现氧化性也表现还原性 |
D | 反应①中氢原子失去电子 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是( ) 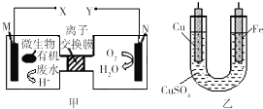
A.质子透过离子交换膜由右向左移动
B.铜电极应与X相连接
C.M电极反应式:(C6H10O5)n+7nH2O﹣24ne﹣═6nCO2↑+24nH+
D.当N电极消耗0.2 mol气体时,则铁电极增重16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O
(1)请用“双线桥法”标出电子转移的方向和数目:。
(2)As2O3在上述反应中________。
A.被氧化
B.被还原
C.既被氧化又被还原
D.既未被氧化又未被还原
(3)该反应的氧化产物是 , 氧化剂是。
(4)若生成0.1 mol AsH3 , 则转移的电子数为。(用NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在消除环境污染领域有广泛的应用.工业上常采用如图所示电解装置,利用铁的化合物中[Fe(CN)6]3﹣可将气态废弃物中的硫化氢转化为可利用的硫,自身转化为[Fe(CN)6]4﹣ . 通电电解,然后通入H2S加以处理,下列说法不正确的是( ) 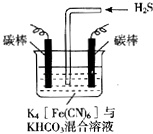
A.电解时阳极反应式为[Fe(CN)6]4﹣﹣e﹣=[Fe(CN)6]3﹣
B.电解过程中阴极区溶液的pH变大
C.整个过程中需要不断补充K4[Fe(CN)6]与KHCO3
D.通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3﹣+2CO32﹣+H2S=2[Fe(CN)6]4﹣+2HCO3﹣+S↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所学知识回答下列问题:
(1)已知常温时红磷比白磷稳定,比较下列反应中△H的大小:△H1△H2 .
①P4(白磷,s)+5O2(g)═2P2O5(s)△H1
②4P(红磷,s)+5O2(g)═2P2O5(s)△H2
(2)已知:稀溶液中,H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJmol﹣1 , 则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量57.3kJ.
(3)已知:C3H8(g )═CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJmol﹣1
CH3CH=CH2(g)═CH4(g)+HC≡CH(g)△H2=32.4kJmol﹣1
则相同条件下,反应C3H8(g)═CH3CH=CH2 (g)+H2(g)的△H=kJmol﹣1
(4)如图是一种钠硫高能电池的结构示意图,M由Na2O和Al2O3制得,其作用是导电和隔膜,该电池反应为2Na+xS=Na2Sx . 该电池正极的电极反应式为 .
用该电池作电源进行铁件镀铜时,若电镀池中两电极的质量开始相同,电镀完成后取出洗净、烘干、称量,二者质量差为25.6g,则理论上该电池负极消耗的质量为g.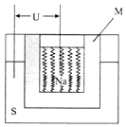
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2mol A与2mol B混合于2L的密闭容器中反应:2A(g)+3B(g)2C(g)+zD(g)若2s后,A的转化率为50%,测得v(D)=0.25molL﹣1s﹣1 , 下列推断正确的是( )
A.v(C)=0.2 molL﹣1s﹣1
B.z=3
C.B的转化率为25%
D.C的体积分数为28.6%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确定Na2CO3和NaHCO3混合物样品的组成,称取四份该样品溶于水后分别滴加相同浓度盐酸30.0mL,充分反应,产生CO2的体积(已折算成标准状况下的体积,不考虑CO2在水中的溶解)如表.
实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
盐酸体积(mL) | 30.0 | 30.0 | 30.0 | 30.0 |
样品质量(g) | 2.96 | 3.70 | 5.18 | 6.66 |
CO2的体积(mL) | 672 | 840 | 896 | 672 |
(1)样品中物质的量之比n(Na2CO3):n(NaHCO3)=;
(2)盐酸的物质的量浓度c(HCl)= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com