
| A. | C、N、Cl | B. | F、O、H | C. | S、P、Si | D. | Na、Mg、Al |
分析 主族元素的最高正价=最外层电子数=主族的族序数,注意F、O元素没有最高正价,据此分析.
解答 解:A.C、N、Cl,最外层电子数依次为4、5、7,C元素最高正化合价为+4,N元素最高正化合价为+5,Cl元素最高正化合价为+7,故A不符合;
B.F、O、H,最外层电子数依次为7、6、1,但是F、O元素没有最高正价,故B不符合;
C.S、P、Si,最外层电子数依次为6、5、4,元素最高正价分别为+6、+5、+4,故C符合;
D.Na、Mg、Al,最外层电子数依次为1、2、3,元素最高正化合价分别为+1、+2、+3,故D不符合,
故选C.
点评 本题考查原子结构与性质关系,难度不大,注意主族元素最高正化合价=最外层电子数=主族族序数,但氧、氟元素没有最高正价.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L苯含有的分子数为0.1nA | |
| B. | 25℃时,PH=13的Ba(OH)2的溶液中含有OH-的数目为0.2nA | |
| C. | 1L0.1mol•L-1Al2(SO4 )3的溶液Al3+的数目为0.2nA | |
| D. | 1.5molNO2与足量H2O反应,转移的电子数为nA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝和硝酸溶液反应 | B. | Fe(OH)3溶液和硫酸反应 | ||
| C. | 氢氧化钡溶液和稀硫酸 | D. | KOH溶液和稀硝酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
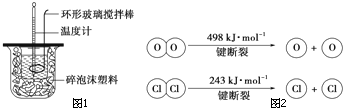 针对化学反应中的能量变化解决下列问题.
针对化学反应中的能量变化解决下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属氧化物都是强电解质 | |
| B. | 一种金属元素只能有一种氧化物 | |
| C. | 在化学反应中,一定有化学键的断裂和形成,并伴有能量的变化 | |
| D. | 能与金属铝反应产生氢气的溶液一定是酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A沸点比B高 | |
| B. | A相对密度比B小 | |
| C. | 一般情况下,同碳原子的烷烃的沸点和密度低于烯烃 | |
| D. | 已知A在常温下为液态,则B不可能为气态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 炒菜时放入食盐并不破坏NaCl中的化学键 | |
| B. | HCl的电子式是 | |
| C. | NaCl熔化时破坏共价键 | |
| D. | HCl的结构式是H-Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com