
| A、一定条件下,水由气态变成液态 |
| B、Ag+(aq)+Cl-(aq)=AgCl(s) |
| C、4NO2(g)+O2(g)═2N2O5 (g) |
| D、火柴盒中的火柴散落到地上 |
科目:高中化学 来源: 题型:
| U | ||
| Y |
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入He的物质的量 | 加入甲的物质的量 |
| y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时的甲的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
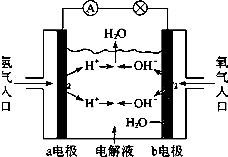
| A、a电极是负极 |
| B、电子从b电极流向a电极 |
| C、在电池工作中,a电极附近pH值降低 |
| D、b电极的电极反应为:4OH--4e-═2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应必然伴随发生能量变化,其能量变化主要是由化学键变化引起的 |
| B、化学反应中能量变化的大小与反应物的质量多少无关 |
| C、101kPa下,1mol的纯物质完全燃烧生成稳定的氧化物时的反应热叫燃烧热 |
| D、酸碱稀溶液中和生成1mol水时的反应热叫中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
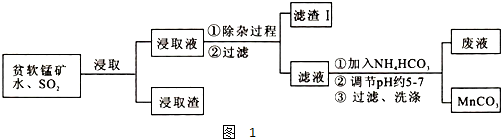
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化铝 | 3.3 | 5.2 |
| 氢氧化亚铁 | 7.6 | 9.6 |
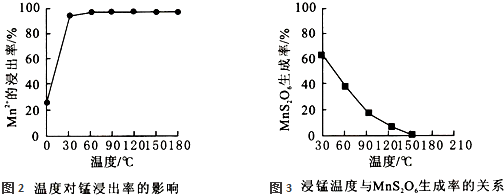
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称量前先调节托盘天平的零点 |
| B、潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量 |
| C、用托盘天平只能称量至0.1g |
| D、称量时左盘放被称量物,右盘放砝码 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 molH2的质量是1 g |
| B、1 mol HCl的质量是36.5 g?mol-1 |
| C、Cl2的摩尔质量等于它的相对分子质量 |
| D、硫酸根离子的摩尔质量是96 g?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com