
【题目】硝酸铝是一种常用皮革鞣剂.工业上用铝灰(主要含Al、A12O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3﹒nH2O]的流程如下:
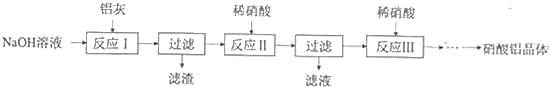
完成下列填空:
(1)用NaOH固体配制30%的NaOH溶液,所需的玻璃仪器除烧杯外,还有______。
a.容量瓶 b.量筒 c.烧瓶
(2)反应Ⅱ中为避免铝的损失,需要解决的问题是______。
(3)从反应Ⅲ所得溶液中得到硝酸铝晶体的步骤依次是:减压蒸发、______、过滤、______、低温烘干.
(4)有人建议将反应Ⅱ、Ⅲ合并以简化操作,说明工业上不采用这种方法的原因______。
(5)某同学在实验室用铝灰制各硝酸铝晶体,其流程如下:
氢氧化物 | Fe(OH)3 | Al(OH)3 |
开始沉淀pH | 1.9 | 4.2 |
沉淀完全pH | 3.2 | 5.4 |
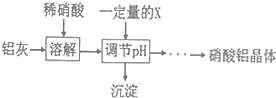
调节pH的目的是______,为使得到的硝酸铝晶体较纯净,所用的X物质可以是______(填编号)。
A.氨水 B.铝 c.氢氧化铝 D.偏铝酸钠
(6)该实验室制法与工业上制法相比,其缺点是______。
(7)称取7.392g硝酸铝晶体样品,加热灼烧使其分解完全,最终得到1.020gAl2O3,计算硝酸铝晶体样品中结晶水的数目为______。
【答案】b 如何控制反应终点(或硝酸的用量 冷却结晶 洗涤 产物中杂质NaNO3的含量较高 将Fe3+转化为Fe(OH)3沉淀除去 BC 产生大量污染性气体NO等 8.7
【解析】
铝灰用氢氧化钠溶液溶解,铝、氧化铝反应生成偏铝酸钠,氧化铁不反应,过滤分离,滤液中含有偏铝酸钠、未反应的NaOH,加入硝酸中和未反应的氢氧化钠,并将偏铝酸钠转化为氢氧化铝沉淀,再过滤分离,氢氧化铝沉淀再用硝酸溶解,得到硝酸铝溶液,经过减压蒸发得到硝酸铝晶体。
(1)用天平称量氢氧化钠,用量筒量取水的体积,在烧杯中溶解,并用玻璃棒搅拌,还需要量筒,故答案为:b;
(2)硝酸属于强酸,可以溶解氢氧化铝沉淀,导致Al元素损失,需要解决的问题是:如何控制反应终点(或硝酸的用量),可以将加入稀硝酸改为通入过量CO2,避免氢氧化铝沉淀溶解,故答案为:如何控制反应终点(或硝酸的用量);
(3)从反应Ⅲ所得溶液中得到硝酸铝晶体的步骤依次是:减压蒸发、冷却结晶、过滤、洗涤、低温烘干,故答案为:冷却结晶、洗涤;
(4)反应Ⅱ、Ⅲ合并以简化操作,产物中杂质NaNO3的含量较高,故答案为:产物中杂质NaNO3的含量较高;
(5)铝灰用稀硝酸溶解,Al、A12O3、Fe2O3均反应得到硝酸铝、硝酸铁,加入X调节pH使铁离子转化为氢氧化铁沉淀,过滤除去;加入的X能与酸反应且不能引入新杂质,故不能选氨水、偏铝酸钠,可以选择Al与氢氧化铝,故答案为:将Fe3+转化为Fe(OH)3沉淀除去;BC;
(6)Al与稀硝酸反应会生成NO,污染空气,故答案为:产生大量污染性气体NO等;
(7)硝酸铝晶体分解得到氧化铝、水,另外物质相当于N2O5,氧化铝的物质的量为![]() =0.01mol,根据Al元素守恒,硝酸铝的物质的量为0.02mol,根据N原子守恒,可知N2O5为
=0.01mol,根据Al元素守恒,硝酸铝的物质的量为0.02mol,根据N原子守恒,可知N2O5为![]() =0.03mol,其质量为0.03mol×108g/mol=3.24g,故结晶水为质量为7.392g﹣1.02g﹣3.24g=3.132g,结晶水物质的量为
=0.03mol,其质量为0.03mol×108g/mol=3.24g,故结晶水为质量为7.392g﹣1.02g﹣3.24g=3.132g,结晶水物质的量为![]() =0.174mol,故结晶水数目为
=0.174mol,故结晶水数目为![]() =8.7,故答案为:8.7。
=8.7,故答案为:8.7。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图所示是探究发生腐蚀的装置图。发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升。下列说法不正确的是

A. 两种腐蚀负极的电极反应式均为Fe-2e-=Fe2+
B. 开始时发生的是析氢腐蚀
C. 一段时间后发生的是吸氧腐蚀
D. 析氢反应的总反应式为2Fe+O2+2H2O=2Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置测定中和热的实验步骤如下:

①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)如图所示,仪器A的名称是_______________;
(2)NaOH溶液稍过量的原因 ______________。
(3)加入NaOH溶液的正确操作是_______(填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是 _________________________。
(5)实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)______
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3-羟基丁酸(3-hydroxybutyrate)也称为β-羟基丁酸(beta-hydroxybutyrate),在工业中可用于合成可生物降解的塑料,如聚(3-羟基丁酸)。
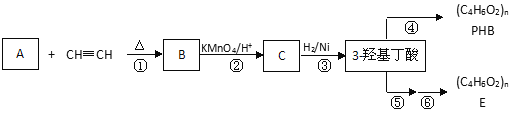
已知:i. 共轭二烯烃(如异戊二烯)与含有碳碳叁键的有机物作用时能形成环状化合物:
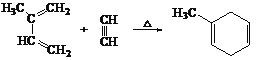
ii. 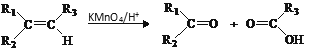
iii. 步骤②只有一种产物;E的结构中含有甲基
(1)A分子结构简式 _______;理论上B也可以由1,3-丁二烯与烃F来合成,则F的名称(系统命名法):_________;C中含有的官能团是_______(用符号表示)。
(2)写出反应类型:②_____________, ④_____________。
(3)PHB______(填“有”或“无”)固定熔沸点;它与E______(填“互为”或“不互为”)同分异构体。下列有机物具有类似共轭二烯烃性质的是__________(填序号);
a. ![]() b.
b. ![]()
c. ![]() d.
d. 
(4)写出反应⑤的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是
A. 向0.1 mol·L1 Na2CO3溶液中通入适量CO2气体后:c(Na+)=2[c(![]() )+c(
)+c(![]() )+c(H2CO3)]
)+c(H2CO3)]
B. 常温下,pH=6的NaHSO3溶液中:c(![]() )c(H2SO3)=9.9×107 mol·L1
)c(H2SO3)=9.9×107 mol·L1
C. 等物质的量浓度、等体积的Na2CO3和NaHCO3混合:![]() <
<![]()
D. 0.1 mol·L1 Na2C2O4溶液与0.1 mol·L1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(![]() )+c(
)+c(![]() )+c(OH)=c(Na+)+c(H+)
)+c(OH)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通电解精炼铜的方法所制备的铜中仍含杂质,利用下面的双膜( 阴离子交换膜和过滤膜)电解装置可制备高纯度的Cu。下列有关叙述正确的是

A. 电极a为粗铜,电极b为精铜
B. 甲膜为过滤膜,可阻止阳极泥及漂浮物杂质进入阴极区
C. 乙膜为阴离子交换膜,可阻止杂质阳离子进入阴极区
D. 当电路中通过1mol电子时,可生成32g精铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是一些物质的熔沸点数据(常压):
钾 | 钠 | Na2CO3 | 金刚石 | 石墨 | |
熔点(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
沸点(℃) | 774 | 882.9 | 1850(完全分解产生CO2) | --- | 4250 |
金属钠和CO2在常压、890℃发生如下反应:4Na(g)+3CO2(g) ![]() 2Na2CO3(1)+C(s,金刚石);△H= —1080.9 kJ/mol
2Na2CO3(1)+C(s,金刚石);△H= —1080.9 kJ/mol
(1)上述反应的平衡常数表达式为________________;若4v正(Na)=3v逆(CO2),反应是否达到平衡________ (选填“是”或“否”)。
(2)若反应在10L密闭容器、常压下进行,温度由890℃升高到1860℃,若反应时间为10min,金属钠的物质的量减少了0.2mol,则10min里CO2的平均反应速率为________________。
(3)高压下有利于金刚石的制备,理由_____________________________________________。
(4)由CO2(g)+4Na(g)=2Na2O(s)+C(s,金刚石) △H= —357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(1)的热化学方程式:___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。
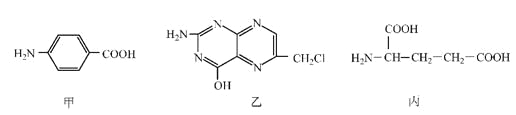
(1)甲中显酸性的官能团是_______________(填名称)。
(2)下列关于乙的说法正确的是__________________(填序号)。
a.分子中碳原子与氮原子的个数比是7:5 b.属于芳香族化合物
c.既能与盐酸又能与氢氧化钠溶液反应 d.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,丁的结构简式为________________。
a.含有![]() b.在稀硫酸中水解有乙酸生成
b.在稀硫酸中水解有乙酸生成
(4)甲可以通过下列路线合成(分离方法和其他产物已经略去):
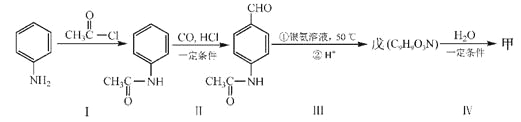
①步骤I的反应类型是______________________。
②步骤I和Ⅳ在合成甲过程中的目的是____________________。
③步骤Ⅳ反应的化学方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:FeCl3(aq)+3KSCN(aq)![]() 3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是
3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是
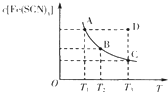
A.A点与B点相比,A点的c(Fe3+)大
B.加入KCl固体可以使溶液由D点变到C点
C.反应处于D点时,一定有υ(正)<υ(逆)
D.若T1、T2温度下的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com