
【题目】某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
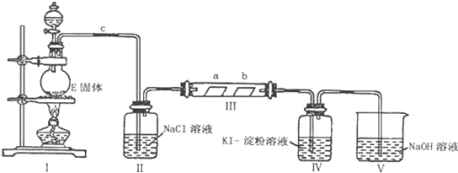
(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是___。
(2)装置Ⅱ的作用是___。
(3)实验过程中,装置IV中的实验现象为___;发生反应的化学方程式为___。
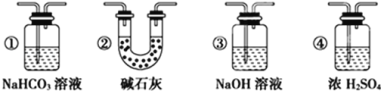
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的___装置(填序号),该装置的作用是___。
(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式___。
【答案】MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O 除去氯气中的氯化氢气体 无色溶液变蓝色 Cl2+2KI=I2+2KCl ④ 干燥Cl2 Cl2+2OH-=Cl-+ClO-+H2O
【解析】
从装置图中看,Ⅰ为制取氯气的装置,Ⅱ为除去氯气中氯化氢的装置,Ⅲ为检验氯气漂白性的装置,Ⅳ为检验氯气氧化性的装置,Ⅴ为尾气处理装置。
(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O。答案为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)装置Ⅱ的作用是除去氯气中的氯化氢气体。
答案为:除去氯气中的氯化氢气体
(3)实验过程中,装置IV中的实验现象为无色溶液变蓝色。
答案为:无色溶液变蓝色
发生反应的化学方程式为Cl2+2KI=I2+2KCl。
答案为:Cl2+2KI=I2+2KCl
(4)因为氯气没有干燥,所以干燥的品红试纸也褪色,为了达到预期目的,应给氯气干燥,也就是在上图装置Ⅱ与Ⅲ之间添加干燥装置。
装置①中,NaHCO3会吸收Cl2,不合题意;
装置②中,碱石灰能与Cl2发生反应,不合题意;
装置③中,NaOH溶液能与Cl2发生反应,不合题意。
装置④中,浓硫酸不仅能吸收水蒸气,而且与Cl2不反应,符合题意;
所以应选择图中的④装置。答案为:④
该装置的作用是干燥Cl2。答案为:干燥Cl2
(5)装置Ⅴ的目的是防止尾气污染,发生反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O。
答案为:Cl2+2OH-=Cl-+ClO-+H2O


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是( )
A. 2p和3p轨道形状均为哑铃形,能量也相等
B. 氮原子的价电子排布图:![]()
C. 利用手性催化剂合成可得到一种或主要得到一种手性分子,手性异构体性质相同
D. 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镇咳药沐舒坦可由化合物甲和化合物乙在一定条件下制得:
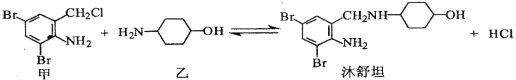
下列有关叙述正确的是( )
A. 甲的分子式为C7H4NBr2Cl
B. 沐舒坦分子中最多有13个碳原子共平面
C. 乙遇FeCl3溶液显紫色
D. 反应过程中加入适量K2CO3可提高沐舒坦的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)现有四种有机物:①乙烯,②2-丙醇,③甲苯,④![]() ,⑤
,⑤![]() ,⑥
,⑥ ,⑦
,⑦![]() ,⑧
,⑧![]() 其中:
其中:
(1)能衡量一个国家的石油化工生产水平的是__________(填序号),该物质可用于制备常用塑料,其反应化学方程式是_______________________。
(2)能用来制取梯恩梯(TNT)的是________(填序号),其发生反应的化学方程式是__________________;
(3)上述有机物能与金属钠发生反应的是_________(填序号),与⑧互为同分异构体的是___________(填序号),⑤与酸性高锰酸钾反应的产物是______________(填结构简式);
(二)实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图所示(铁架台、铁夹、酒精灯等未画出):
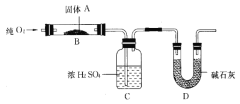
取17.1g A放入B装置中,持续通入过量O2燃烧,生成CO2和H2O,请回答下列有关问题:
(4)D装置的作用是____________________,有同学认为该套装置有明显的缺陷,需要改进,该同学判断的理由是___________________;
(5)装置改进后进行实验,若A的摩尔质量为342g/mol,C装置增重9.9g,D装置增重26.4 g,则A的分子式为_____________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应涉及到H2O、ClO-、NH4+、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法正确的是
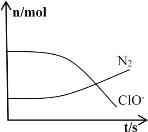
A. 该反应中Cl-为氧化产物
B. 消耗1mol还原剂,转移6mol电子
C. NH4+被ClO-氧化成N2
D. 反应后溶液的酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行):
![]()
Ⅰ.若A为有刺激性气味的气体,水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
(1)A的电子式为___。
(2)A的催化氧化反应的化学方程式为__。
Ⅱ.若A、C、W都是常见气体,C是导致酸雨的主要气体,常温下A与C反应生成B,
(1)A与C反应生成B的化学方程式为___。
(2)某化学活动小组将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:___。
Ⅲ.A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。则C的化学式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:
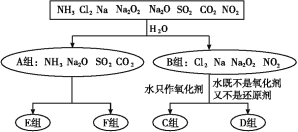
(1)上述分类中,分成A、B两组的依据是_________。
(2)D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有__(填化学式)。
(3)实验室由Al3+制备Al(OH)3时,应选择F组中_____(填化学式)的水溶液,离子方程式为______。
(4)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式___,②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组采用下图所示装置进行Fe粉与水蒸气的反应。

(1)实验前检查装置气密性的方法为______________。
(2)检验实验中生成气体的实验操作是 _____________。
(3)写出试管中发生的化学反应方程式________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com