
【题目】下列物质分类正确的是( )
A.SO2、SiO2、CO均为酸性氧化物 B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质 D.福尔马林、水玻璃、氨水均为混合物
科目:高中化学 来源: 题型:
【题目】下列装置适用于实验室制氨气并验证氨气的某化学性质,其中能达到实验目的的是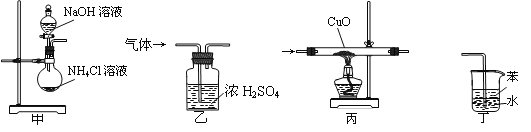
A.用装置甲制取氨气 B.用装置乙除去氨气中的水蒸气
C.用装置丙验证氨气具有还原性 D.用装置丁吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应:
①A+H2O―→B+C ②C + F―→D
③D+NaOH![]() F+E+H2O
F+E+H2O
(1)写出它们的化学式:
C________,D________,E________。
(2)写出各步反应的离子方程式:
①_______________________________________________________________;
③_______________________________________________________________。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O。写出该步反应的化学方程式:____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明乙酸是弱酸的实验事实是
A.CH3COOH溶液与Zn反应放出H2
B.0.1mol/L CH3COONa溶液的pH大于7
C.CH3COOH溶液与NaCO3反应生成CO2
D.0.1 mol/L CH3COOH溶液可使紫色石蕊变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,回答下列问题:
主族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0族 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(1)元素①的名称是_____________;比元素⑧质子数多10的元素在周期表中所处位置___________。
(2)元素③的单质的电子式为_____________,元素③的气态氢化物与其最高价氧化物的水化物反应的化学方程式为_________________________________________。
(3)用电子式表示元素⑨与⑥的化合物的形成过程:____________________________,该化合物属于__________(填“共价或“离子”)化合物。
(4)表示②与⑦形成的化合物的电子式:________________________,该化合物是由__________(填“极性”或“非极性”)键形成的。
(5)元素⑥的氢化物的结构式为_____________________;该氢化物常温下和元素⑦的单质反应的化学方程式为________________________________;元素③④⑥形成的氢化物沸点由高到底的顺序(写化学式)___________________________。
(6)④、⑥、⑦、⑨四种元素形成的简单离子,离子半径由大到小的顺序是(写离子符号)__________________________________。
(7)某原子有6个电子、7个中子,写出其元素符号:________________________。
(8)④⑥可与氢元素构成多种10电子和18电子的粒子,其中符合下列要求的粒子的电子式为:4核18电子的分子_____________________,10电子的阳离子_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1mol XY2含有54mol电子。
(1)该融雪剂的化学式是____________;X与氢元素形成的化合物的电子式是_______________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是____________;D与E能形成一种结构类似CO2的三原子分子,且每个原子均达到8e稳定结构,该分子的结构式为________________。
(3)Z与Y同主族,Z、Y位于相邻周期,且Z的原子半径大,则Z单质常温下呈_____态(填“气”“液”或“固”)。
(4)元素W与D同主族,且W与D可形成两种常见化合物,其中能使品红溶液褪色的是____________(填化学式),写出其与Z单质的水溶液反应的化学方程式:____________________。
(5)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2(R为1价),该反应的离子方程式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构如图所示,这种有机物不可能具有的性质是

①可以与氢气发生加成反应;②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;④能发生酯化反应;
⑤能发生加聚反应;⑥能发生水解反应
A. ①④ B. 只有⑥ C. 只有⑤ D. ④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的化合物在生产生活中有广泛应用。
(1)硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如下:

① 上述流程中采用稀碱液比用热水更好,理由是__________________。
② 取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)=______mol·L-1。(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
(2)工业上常利用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3。KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g 成品溶于水并加入淀粉做指示剂,再用0.01000 mol·L1 KIO3酸性标准溶液滴定至终点,消耗KIO3溶液31.25mL。
① 滴定终点观察到的现象为:_____________________。
② 成品中Na2SO3的质量分数是_________(请写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】湿法炼锌产生的铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。一种由铜镉渣生产金属镉的流程如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol/L计算):
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,其离子方程式是__________________。
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3。该微电池的正极反应式为_____。
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH。
① 除铁过程中,理论上参加反应的物质n(KMnO4)∶n(Fe2+)=_________。
② 除铁时加入ZnO控制反应液pH的范围为________________。
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:_____________________。
(5)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com