
 2SO3(g) ��H����196kJ/mol����߷�Ӧ��SO2��ת���ʣ��Ǽ���SO2�ŷŵ���Ч��ʩ��
2SO3(g) ��H����196kJ/mol����߷�Ӧ��SO2��ת���ʣ��Ǽ���SO2�ŷŵ���Ч��ʩ��| A��SO2��O2��SO3���ߵ�Ũ��֮��Ϊ2��1��2 | B�������������ѹǿ���� |
| C�������ڻ��������ܶȱ��ֲ��� | D��SO3�����ʵ������ٱ仯 |
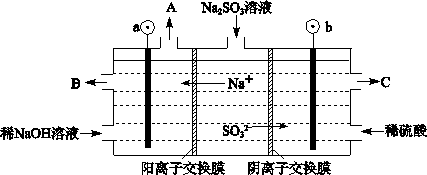


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CaO(s) + SO2(g) + CO2(g) ��H1=218.4kJ��mol-1(��Ӧ��)
CaO(s) + SO2(g) + CO2(g) ��H1=218.4kJ��mol-1(��Ӧ��)  CaS(s) + 4CO2(g) ��H2= -175.6kJ��mol��1(��Ӧ��)
CaS(s) + 4CO2(g) ��H2= -175.6kJ��mol��1(��Ӧ��)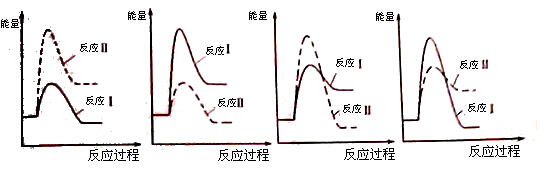
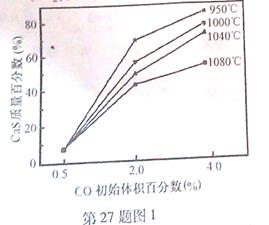
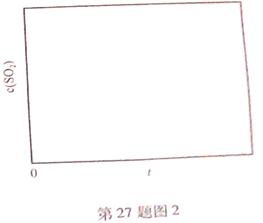
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
 CH3OH+H2O����ش��������⣺
CH3OH+H2O����ش��������⣺
|
|
|
|
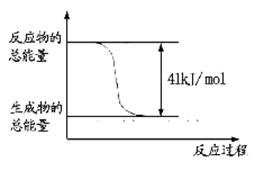
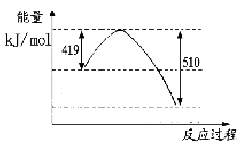 д���ɶ�����̼�������Ʊ��״����Ȼ�ѧ����ʽ__ _��
д���ɶ�����̼�������Ʊ��״����Ȼ�ѧ����ʽ__ _��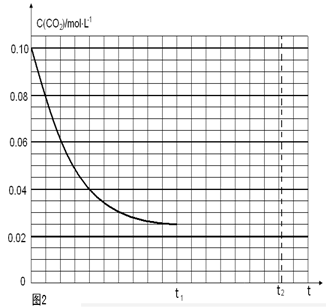
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���

 ��_________���ƶ���
��_________���ƶ��� ��һ���¶��£���2 L�ݻ�������ܱ������г���4 mol
��һ���¶��£���2 L�ݻ�������ܱ������г���4 mol  ��6 mo1 H2O(g)������Ӧ��10 minʱ����Ӧ�ﵽƽ��״̬�����CH4(g)��H2(g)�����ʵ�����ʱ��仯��������ͼ��ʾ��
��6 mo1 H2O(g)������Ӧ��10 minʱ����Ӧ�ﵽƽ��״̬�����CH4(g)��H2(g)�����ʵ�����ʱ��仯��������ͼ��ʾ��
 (CO)��ʾ�Ļ�ѧ��Ӧ����Ϊ_________��
(CO)��ʾ�Ļ�ѧ��Ӧ����Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3(g)����H��0
2SO3(g)����H��0
| A�����˴������� | B����С������� | C�������¶� | D������SO3�����ʵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Ni��CO��4��g��
Ni��CO��4��g��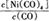 ������?H 0���>����<������
������?H 0���>����<������
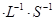 ��
��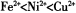 )
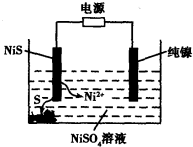
)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 4NO��6H2O�����ڷ�Ӧ��ʼ��5s��10s֮��ķ�Ӧ���ʷֱ���v(NH3)��v(O2)��v(NO)��v(H2O)��ʾ���������ж���ȷ�Ĺ�ϵ��(����)��
4NO��6H2O�����ڷ�Ӧ��ʼ��5s��10s֮��ķ�Ӧ���ʷֱ���v(NH3)��v(O2)��v(NO)��v(H2O)��ʾ���������ж���ȷ�Ĺ�ϵ��(����)��A��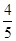 v(NH3)��v(O2) v(NH3)��v(O2) | B��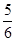 v(O2)��v(H2O) v(O2)��v(H2O) |
C��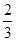 v(NH3)��v(H2O) v(NH3)��v(H2O) | D��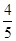 v(O2)��v(NO) v(O2)��v(NO) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��v(O2)��3��2g��L��1��min��1 | B��v(O2)��0��1 mol��L��1��min��1 |
| C��v(KCl)��0��1 mol��L��1��min��1 | D��v(KClO3)��0��0667 mol��L��1��min��1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com