
| A���ⶨHCl��NaOH���к���ʱ��ÿ��ʵ���Ӧ���������¶ȣ���������ʼ�¶ȡ�NaOH��ʼ�¶Ⱥͷ�Ӧ�����ֹ�¶� |
| B���ɡ�C��ʯī��=C�����ʯ������H=" +119" kJ/mol ����֪���ʯ��ʯī�ȶ� |
| C����ϡ��Һ�У� H+��OH����H2O����H����57.3kJ/mol��������0.5molH2SO4��Ũ�����뺬1molNaOH����Һ��ϣ��ų�����������57.3kJ |
| D����101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2(g)+O2(g)=2H2O(l)����H= +285.8kJ/mol |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
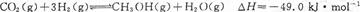
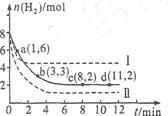
| A��O��1 min | B��1��3 min | C��3��8 min | D��8��11 min |
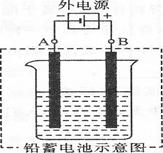
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
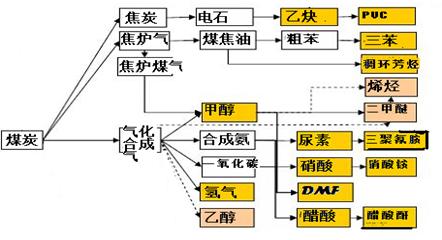
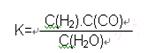
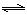 2CO��g����K1
2CO��g����K1 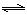 H2��g��+CO2��g����K2
H2��g��+CO2��g����K2 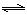 CO��g��+H2��g����K3
CO��g��+H2��g����K3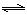 H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
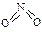 ��
��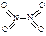 ����֪N��N������Ϊ167kJ��mol��1��NO2�е������ļ���Ϊ466kJ��mol��1��N2O4�е������ļ���Ϊ438.5kJ��mol��1����д��NO2ת��ΪN2O4���Ȼ�ѧ����ʽΪ ��
����֪N��N������Ϊ167kJ��mol��1��NO2�е������ļ���Ϊ466kJ��mol��1��N2O4�е������ļ���Ϊ438.5kJ��mol��1����д��NO2ת��ΪN2O4���Ȼ�ѧ����ʽΪ ��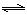 2NO2(g)�����¶�ΪT1
2NO2(g)�����¶�ΪT1 ��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ��
��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ��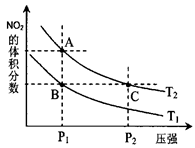
 ��ķ�Ӧ���ʣ�A��C
��ķ�Ӧ���ʣ�A��C �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ж���
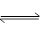 2SO3��Ϊ���淴Ӧ����ش�
2SO3��Ϊ���淴Ӧ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 N2+2CO2��
N2+2CO2�� N2��g��+2CO2��g����Ӧ��ƽ�ⳣ���ı���ʽΪ��
N2��g��+2CO2��g����Ӧ��ƽ�ⳣ���ı���ʽΪ��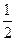 O2��g��=2CO2��g�� ��H=һ283 kJ��mol
O2��g��=2CO2��g�� ��H=һ283 kJ��mol N2��g��+2CO2��g����H= kJ��mol��
N2��g��+2CO2��g����H= kJ��mol�� N2��g��+2CO2��g������ϣ�2������Ϣ������˵����ȷ���� ��
N2��g��+2CO2��g������ϣ�2������Ϣ������˵����ȷ���� �� ����
�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH��g�� ��H1
CH3OH��g�� ��H1 CH3OH��g�� + H2O��g�� ��H2
CH3OH��g�� + H2O��g�� ��H2| �¶� | 250�� | 300�� | 350�� |
| K | 2��041 | 0��270 | 0��012 |
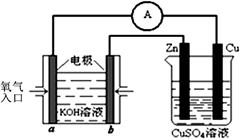
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
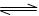 2NH3 (g) ��H<0�����з�����ȷ���� �� ��
2NH3 (g) ��H<0�����з�����ȷ���� �� ��| A��ƽ������N2���÷�Ӧ�ġ�H���� |
| B����ƽ��������¶ȣ���ƽ�ⳣ��K��� |
| C��ƽ����ٳ���NH3���ﵽ��ƽ��ʱ��NH3�İٷֺ������ |
| D������Ӧǰ���˵�N2��H2���ʵ�����ȣ���ƽ��ʱN2��ת���ʱ�H2�ĸ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com