
【题目】FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
A.溶液中一定含Cu2+B.溶液中一定含Fe2+
C.剩余固体一定含CuD.加入KSCN溶液一定不变红色
科目:高中化学 来源: 题型:
【题目】下列关于常见化学物质的应用不正确的是( )
A.干冰能用作冷冻剂
B.明矾可用作净水剂
C.味精可用作食品调味剂
D.苏打是一种膨松剂,可用于制作馒头和面包
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应属于加成反应的是( )
A.CH3CH3+Cl2 ![]() CH3CH2Cl+HCl
CH3CH2Cl+HCl
B.CH2═CH2+HBr→CH3CH2Br
C.2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D.CH3COOH+CH3CH2OH ![]() H3COOCH2CH3+H2O
H3COOCH2CH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性小组为了探究石蜡油分解产物,设计了如下实验方案。下列说法错误的是
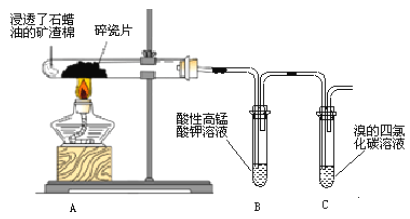
A. 碎瓷片有催化和积蓄热量的作用
B. 结束反应时,先撤出导管,再停止加热
C. 石蜡油是液态烷烃
D. B、C中溶液均褪色,反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在四个恒容密闭容器中按下表相应量充入气体,发生反应2N2O(g) ![]() 2N2(g)+O2(g),容器I、II、III中N2O的平衡转化率如下图所示:
2N2(g)+O2(g),容器I、II、III中N2O的平衡转化率如下图所示:
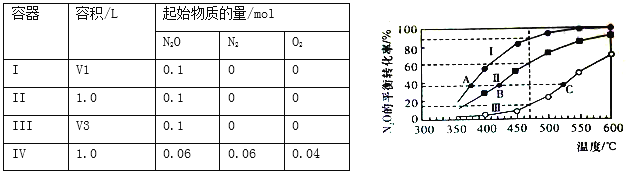
下列说法正确的是
A. 该反应的正反应放热
B. 相同温度下反应相同时间,平均反应速率:v(I)>v(II)
C. 容器IV在470℃进行反应时,起始速率:v正(N2O)<v逆(N2O)
D. 图中A、B、C三点处容器内总压强:pA(I)<pB(II)<pC(III)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.反应Fe+H2S04=FeS04+H2↑的能量变化趋势,如图所示:

(1)该反应为______反应(填“吸热”或“放热”)。
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______极(填“正”或“负”)。铜片上产生的现象为_____________,该极上发生的电极反应为____________,
II.在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g)=3C(g)+nD(g),开始时 A为4mol, B为6 mol, 5min末时测得C的物质的量为3mol,用D表示的化学反应速率![]() (D)为 0.2 mol/(Lmin).
(D)为 0.2 mol/(Lmin).
计算:
(1)5 min末A的物质的量浓度为_________。
(2)前5 min 内用B表示的化学反应速率![]() (B))为__________。
(B))为__________。
(3)化学方程式中n的值为_________。
(4)此反应在四种不同情况下的反应速率分别为:

其中反应速率最快的是________(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积恒定的密闭容器中,一定量的SO2与1.25molO2在催化剂作用下加热到600℃发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)△H<0 。30s气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%。下列有关叙述正确的是
2SO3(g)△H<0 。30s气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%。下列有关叙述正确的是
A. 达到平衡时,气体的密度是反应前的80%
B. 将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为209.7g
C. 该温度下的平衡常数为101.25L/moL
D. 0~30s时SO3生成速率为3.0×10-2mol/(L.s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO、NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)与氮氧化物有关的全球或区域性大气环境问题有_______(填字母序号)。
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(2)NO2可与水发生反应,反应的化学方程式为__________________。若该反应有0.6NA个电子转移,则参加反应的NO2的物质的量为___________。
(3)NH3也是重要的含氮化合物,请写出实验室中由固体物质制取氨气的化学方程式________________________________;工业上可利用NH3经过一系列反应制取硝酸,请写出NH3在催化剂的作用下,与O2反应的化学方程式_________________________________。
(4)硝酸可与不活泼金属铜发生反应。将过量的铜置入一定量的浓硝酸中,微热,充分反应后,放出1.12 L气体(标准状况下),
①写出反应过程其中1个化学反应的化学方程式:_______________________________。
②整个反应过程中,被还原的HNO3总的物质的量是___________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应:2SO2(g)+O2(g)2SO3(g)△H<0.得到如表中的两组数据:
实验编号 | 温度/℃ | 平衡常数/mol﹣1L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
① | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
② | T2 | K2 | 4 | 2 | 0.4 | y | t |
下列说法不正确的是( )
A.x=1.6,y=0.2,t<6
B.T1、T2的关系:T1>T2
C.K1、K2的关系:K2>K1
D.实验1在前6 min的反应速率v (SO2)=0.2 molL﹣1min﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com