
【题目】乙烯和丙烯是重要有机化工原料。
I.以乙烯为原料可以制备乙二醇和高分子化合物B。
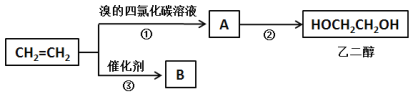
(1)①的化学方程式为______________。
(2)②为取代反应,通过A与NaOH溶液加热条件下完成转化。②的化学反应方程式为__________。
(3)③的反应类型为_______________,B的结构简式为________________。
II.丙烯酸乙酯天然存在于菠萝等水果中,是一种天然香料,也可以由乙烯和丙烯为原料合成。

(4)有机物E中的官能团是_________________。
(5) D与E反应生成丙烯酸乙酯的化学反应方程式为__________________。
(6)下列说法正确的是______________。
a.乙烯、丙烯是石油裂解的产物 b.乙二醇易溶于水
c.E能使酸性高锰酸钾溶液褪色 d.D可以由葡萄糖分解得到
【答案】CH2=CH2+Br2→CH2BrCH2Br CH2BrCH2Br+2H2O![]() HOCH2CH2OH+2HBr 加聚反应
HOCH2CH2OH+2HBr 加聚反应 ![]() 碳碳双键和羧基 CH3CH2OH+CH2=CHCOOH
碳碳双键和羧基 CH3CH2OH+CH2=CHCOOH![]() CH2=CHCOOCH2CH3+H2O abcd
CH2=CHCOOCH2CH3+H2O abcd
【解析】
乙烯可以和溴的四氯化碳反应生成1,2-二溴乙烷,1,2-二溴乙烷发生水解反应生成乙二醇,乙烯在催化剂存在的条件下生成聚乙烯。根据丙烯酸乙酯逆推,A和B反应生成丙烯酸乙酯的反应类型应该是酯化反应;反应物应该为乙醇和丙烯酸;结合题目所给的初始物质的结构简式可知,有机物D为乙醇,有机物E为丙烯酸,据此分析。
(1)①表示的是乙烯和溴的加成反应,化学方程式为CH2=CH2+Br2→CH2BrCH2Br;
(2)②为取代反应,CH2BrCH2Br在NaOH溶液加热条件下发生水解生成醇,化学反应方程式为CH2BrCH2Br+2H2O![]() HOCH2CH2OH+2HBr;
HOCH2CH2OH+2HBr;
(3)③的反应类型为加聚反应,nCH2=CH2![]()
![]() ,B的结构简式为
,B的结构简式为![]() ;
;
(4)有机物E为丙烯酸,结构简式为CH2=CHCOOH,它的官能团为碳碳双键和羧基;
(5)有机物D为乙醇,有机物E为丙烯酸,它们在浓硫酸作催化剂加热的条件下反应生成酯和水,化学反应为:CH3CH2OH+CH2=CHCOOH![]() CH2=CHCOOCH2CH3+H2O;
CH2=CHCOOCH2CH3+H2O;
(6)a.在高温下,将石油产品中具有长链分子的烃断裂为各种短链的气态烃和液态烃称为的裂解,乙烯、丙烯是石油裂解的产物,故a正确;
b.乙二醇含有羟基,水中也含有羟基,乙二醇和水分子之间易形成氢键,故乙二醇易溶于水,故b正确;
c.E为丙烯酸,含有碳碳双键,能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液褪色,故c正确;
d.D为乙醇,可以由葡萄糖发生无氧呼吸得到,故d正确;
答案选abcd。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】氮、硒形成的单质及其化合物有重要的科学研究价值,请回答下列问题:
(1)邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。基态氮原子的价电子轨道表示式为______________;其核外电子共占据____个能级;邻氨基吡啶的铜配合物中Cu2+的配位数是_______。

(2)高聚氮晶体结构如图所示,每个氮原子与另外三个氮原子结合形成空间网状结构。固态高聚氮是_______晶体;该晶体中n(N)与n(N—N)之比为_______;这种高聚氮N—N键的键能为160 kJ·mol-1,而N2的键能为942 kJ·mol-1,其可能潜在的应用是__________。

(3)NO3-的空间构型是________;HNO3的酸性比HNO2强,试从结构的角度解释其原因__________。
(4)硒有三种晶体(α单斜体、β单斜体和灰色三角晶),灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶胞结构图和晶胞俯视图如图所示:

已知正六棱柱的边长为acm,高为bcm,阿伏加德罗常数的值为NA,则该晶体的密度为_____g·cm-3(用含NA、a、b的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是合成抗病毒药品洛匹那韦的一种重要中间体。其合成路线如下(其中Ph表示苯基):

回答下列问题:
(1)物质A的化学名称是_______________
(2)反应①所需的试剂和条件是 ______________;反应⑤所属的反应类型为__________________
(3)F中含氧官能团的名称是_______________
(4)反应②的化学反应方程式为______________
(5)有机物X是C的同分异构体,写出满足下列条件的X结构简式为_______________
①苯环上有三个取代基
②分子结构中含有硝基
③核磁共振氢谱有4组峰,峰面积之比为6:2:2:1
(6)写出以![]() 和CH3CN为原料,制备
和CH3CN为原料,制备 的合成路线(无机试剂任选)。_______________
的合成路线(无机试剂任选)。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
装置图 |
|
|
|
|
现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊 |
结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 | Ksp:AgCl>AgBr>AgI | 非金属性:C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)工业合成氨是制取氮肥的基础。合成氨反应中,反应物 N2 的结构式是_______________,产物NH3 的电子式是_________________。
(2)某小组在实验室模拟以 NH3 为原料, 制备少量硝态氮肥 Ca(NO3)2,转化途径如下(转化所需试剂及条件已略去)。
![]()
①NO→NO2 的现象是______________, NO2→HNO3 的化学方程式为____________________。
②将HNO3 转化为 Ca(NO3)2,列举两种不同类别的化合物 M___________________(写化学式) 。
(3)①NH4HCO3 是一种铵态氮肥,需阴凉处保存,原因是_______________(写化学方程式)。
②实验室检验某化肥是铵态氮肥,检验过程中发生反应的离子方程式为___________________。
(4)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去) 
①X可能是SO3 或_______________,Y是_____________。
②尿素CO(NH2)2是一种常用有机氮肥,缓慢与 H2O 发生非氧化还原反应释放出NH3和另外一种气体,该反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
(1)砷的常见氧化物有 As2O3 和 As2O5,其中 As2O5 热稳定性差。根据图 1 写出 As2O5 分解为 As2O3 的热化学方程式_________________。

(2)砷酸钠具有氧化性,298 K 时,在 100 mL 烧杯中加入 10 mL 0.1 mol/L Na3AsO4 溶液、20 mL 0.1 mol/L KI 溶液和 20 mL 0.05 mol/L硫酸溶液,发生下列反应:AsO43-(无色)+2I-+2H+ ![]() AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中 c(I2)与时间(t)的关系如图 2 所示(溶液体积变化忽略不计)。
AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中 c(I2)与时间(t)的关系如图 2 所示(溶液体积变化忽略不计)。
①下列情况表明上述可逆反应达到平衡状态的是_______(填字母代号)。
a.溶液颜色保持不再变化 b.c(AsO33-)+c(AsO43-)不再变化
c.AsO43-的生成速率等于 I2 的生成速率 d.![]() 保持不再变化
保持不再变化
②0~10 min 内,I的反应速率 v(I)=_______。
③在该条件下,上述反应的平衡常数 K=______。
④升高温度,溶液中 AsO43-的平衡转化率减小,则该反应的 ΔH______0(填“大于”“小于”或“等于”)。
(3)雄黄(As4S4)在空气中加热至 300℃时会生成两种氧化物,其中一种氧化物为剧毒的砒霜(As2O3), 另一种氧化物为______(填化学式),可用双氧水将 As2O3 氧化为 H3AsO4 而除去,写出该反应的化学方 程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对不同有机化合物的系统命名,正确的是 ( )
选项 | A | B | C | D |
物质 |
|
|
| CH3CH2OOCCOOCH2CH3 |
系统命名 | 2- 甲基-2-丁烯 | 2-乙基丁烷 | 3-己酸 | 二乙酸二乙酯 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com