
��15�֣�ʵ�����������᳧����(��Ҫ�ɷ�Ϊ���������P����FeS��SiO2��)�Ʊ�����(��ʽ�������ľۺ���)���̷�(FeSO4��7H2O)���������£�
��1�������̢��еIJ���������ͨ��������Һ�У���Һ����ɫ���� ��
A��Ʒ����Һ B����ɫʯ����Һ C������KMnO4��Һ D����ˮ
��2�����̢��У�FeS��O2��H2SO4��Ӧ�����ӷ���ʽΪ�� ��
��3�����̢��У������������� ��
��4�����̢��У������ᾧ��Ҫʹ�þƾ��ơ����Ǽܡ������ǣ�����Ҫ�������� ��
��5�����̢ݵ���pH��ѡ�������Լ��е� (��ѡ�����)��
A��ϡ���� B��CaCO3 C��NaOH��Һ
��6�����̢��У�����ҺZ���ȵ�70һ80�棬Ŀ���� ��
��7��ʵ����Ϊ�������õ��ľ�����Ʒ����Ԫ�ص�������������������ʵ�顣���÷�����ƽ��ȡ2.700g��Ʒ���ڽ���Ʒ�����������������������Ȼ�����Һ���۹��ˡ�ϴ�ӡ�����������ù�������Ϊ3.495g�����þ�����Ҫ�ɷ�Ϊ[(Fe(OH)(SO4)]n����þ�����Ʒ����Ԫ�ص���������Ϊ ��(���������в�����Ԫ�غ���Ԫ��)��
��1��ACD ��2��4FeS+3O2 + 12H+= 4Fe3++6H2O+4S ��3��Fe(����) ��4������������
��5��C��6���ٽ�Fe3+��ˮ�� ��7��31.1%
���������������1������W�к���S��SiO2,�������ա����е�S���ΪSO2���壬SO2������Ư���ԣ���ʹƷ����Һ��ɫ��SO2�����л�ԭ�ԣ���ʹ����KMnO4��Һ����ˮ����������Ӧ��Ӧ����ɫ������ʹ��ɫʯ����Һ��Ϊ��ɫ�����ѡ��ΪA��C��D����2�����̢��У����ݿ�ͼ�еĸ������ʼ������غ㶨�ɺ͵����غ㡢����غ��֪��FeS��O2��H2SO4��Ӧ�����ӷ���ʽΪ4FeS+3O2 + 12H+= 4Fe3++6H2O+4S����3�����ڷ�����Ӧ�õ��������к���Fe3+.�������Ҫ��ȡ�̷�FeSO4�����Թ��̢��У�Ҫ���뻹ԭ��Fe�ۡ���4�����̢��У������ᾧ��Ҫʹ�þƾ��ơ����Ǽܡ������ǣ�����Ҫ����������������������5�����̢ݵ���pH��ʹ��Һ��pH����Ӧ�ü����ų�A����������CaCO3���������ᣬ�����������������Ca2+�����׳�ȥ����˿�ѡ�������Լ��е�NaOH��ѡ��ΪC����6�����̢��У�����ҺZ���ȵ�70һ80�棬Ŀ���Ǵٽ�Fe3+��ˮ��ʹѸ�ٲ�����������7��n(SO42-)=3.495g��233g/mol=0.015mol��n(Fe)= n(SO42-)= 0.015mol,����m(Fe)=0.015mol��56g/mol=0.84g�����Ըþ�����Ʒ����Ԫ�ص���������Ϊ��0.84g�� 2.700g����100%=31.1%��
���㣺����SO2�����ʡ����ӷ���ʽ����д����ѧʵ�����������Ԫ�ص����������ļ����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�������ˮ���ռ�Ũ�������ȷֽ������������壬��
| A���ռ���NO | B���ռ���NO2 | C���ռ���O2 | D���ռ������κ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����й�������;��˵����ȷ���� (����)
| A���Թܡ��ձ��������ڸ�Һ�塢������� |
| B��ʹʳ��ˮ��NaCl�ᾧ����ʱ���õ����������������ƾ��ơ��������������� |
| C������NaCl��Na2SO4ʱ���õ���ͷ�ιܡ��Թ� |
| D��©�������ڹ��˼���ζ�����������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
��16�֣��Ի�����Ϊԭ��������������������к�Fe2O3��SiO2��Al2O3��MgO�ȣ����������Ʊ����죨Fe2O3���Ĺ������£�
��1�����ܹ�����Fe2O3��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ ��
������A����Ҫ�ɷݵĻ�ѧʽΪ ��
��2����ԭ�����м���FeS2��Ŀ���ǽ���Һ�е�Fe3 +��ԭΪFe2 +��������������ΪH2SO4������ɸ÷�Ӧ�����ӷ���ʽ��FeS2 + 14Fe3 + + H2O="=" 15Fe2 + + SO42- + ��
��3�����������У�O2��NaOH��Fe2+��Ӧ�����ӷ���ʽΪ ��
��4��Ϊ��ȷ�����������������������Ҫ������Һ��pH�ķ�Χ�� ���������ӳ�����pH���±�������ҺB���Ի��յ������У�д��ѧʽ�� ��
| ������ | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| ��ʼ����pH | 2.7 | 3.8 | 7.6 | 9.4 |
| ��ȫ����pH | 3.2 | 5.2 | 9.7 | 12.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
(12��)A-I�ֱ��ʾ��ѧ��ѧ�еij������ʣ�����֮����ת����ϵ����ͼ��ʾ(���ַ�Ӧ�������û���г�)������֪G��һ�����������A��B��C��D��E��F���������о�����ͬһ��Ԫ�أ�FΪ���ɫ������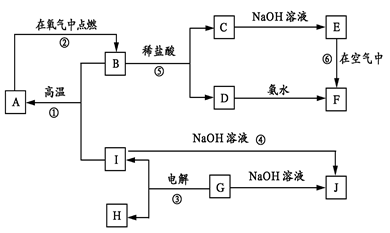
����д���пհף�
��1�� A��B��C��D��E��F����������������ͬһ��Ԫ���� ��дԪ�ط��ţ���
��2�� д������C��G�Ļ�ѧʽ��C ��G ��
��3�� д����Ӧ�١��ܵĻ�ѧ����ʽ����Ӧ�٣� ����Ӧ�ܣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
����ѧѡ��2����ѧ�뼼������15�֣���ҵ������������ʱ����ͬʱ������һ�ֳ�������Ҫ������������Ư����������(NaClO2)���乤���������£�
��֪����NaHSO4�ܽ�����¶ȵ����߶������ʵ� �����¿ɽᾧ������
�ڸ�����������Ϊֹ������֪���е���ǿ�ᣬ�е�90 �档
��ش��������⣺
��Ӧ�����з�����Ӧ�Ļ�ѧ����ʽΪ ����ȴ��Ŀ���� ��������������������ԭ���� ��
��2)��Ӧ�����з�����Ӧ�����ӷ���ʽΪ ��
��3��ͨ�뷴Ӧ�����е�SO2��H2O2����ͬ��������NaClO2�����Ҫ˵��˫��ˮ�ڷ�Ӧ���ܴ���SO2��ԭ���� ��
��4��Ca(ClO)2��ClO2��NaClO2�Ⱥ��Ȼ����ﶼ�dz��õ���������Ư��������Ϊ���Ƕ����� ����д����ҵ����������NaOH��Һ����������NaClO�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
����X��Y�뻯����ס�������ͼ��ʾ��ת����ϵ����Ҫ�ķ�Ӧ����δ��������ش��������⣺
��1�����÷�Ӧ���ڹ�ҵ����ȡ�ֹ裬д����ѧ����ʽ________ ��
��2����X��YΪ�ճ������г��������ֽ������Ҽ�Ϊ����ɫ��ĩ����Ӧ�Ļ�ѧ����ʽΪ___ ���ҷֱ��ܽ��������������NaOH��Һ�У�������������Һ�������ɲ����գ��������ù���Ļ�ѧʽ�ֱ���____ ��____ ��
��3����X������ɫ��Ӧ���ʻ�ɫ������һ�ֳ�������ɫ��ζ��Һ�壬���������������Ļ�ѧ��������____ ��
��4����X�ǻ���ɫ���壬�ס�����������������������̡�����X��Ӧ�Ļ�ѧ����ʽΪ ��
��5�����÷�ӦΪCu+2H2O=Cu��OH��2+H2�������ڴ���ֽ�н���ͼ�������������ɱպϻ�·��ʹ��װ���ܹ��������û���Ӧ������������װ����ʵ�ֵ���Ҫ����ת����ʽΪ ת��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
X��Y��Z��W��Q����Ԫ��ԭ��������������XΪ�ؿ��к�����ߵ�Ԫ�أ������ڱ���Y��X��Z��Q���ڣ�Q��X����ܲ��ϵĵ�������ͬ��Wԭ�Ӻ��������ֲ�ͬ�ܼ��ĵ��ӣ�������ܼ���û��δ�ɶԵ��ӣ�W��X���γ�W2X��WX���ֻ����
�ش��������⣺
��1��X����ԭ��������С��Ԫ���γ�ԭ�Ӹ�����Ϊ1��1�ķ��ӣ��÷��ӵĵ���ʽΪ ��
��2��W2+�ĺ�������Ų�ʽΪ ��
��3��Z����������ˮ��ˮҺ�� ɫ��������ͨ��Y��ij���������Һ��ɫ��ȥ���û�ѧ����ʽ��ʾԭ�� ��
��4��Y��ZԪ�صĵ�һ������Y Z���>������<����=������ X��ؿ��к����ڶ���Ԫ���γɵĻ����������ľ�������Ϊ ��
��5����֪X�ֱ���Ԫ��̼�����γɻ����������·�Ӧ��
2CX��g��+X2(g)=2CX2(g) ��H=��566.0kJ��mol-1
N2(g)+X2(g)="2NX(g)" ��H=189.5kJ��mol-1
2NX(g)+X2(g)=2NX2(g) ��H=��112.97kJ��mol-1
д��NX2��CX��Ӧ���ɴ����д��ڵ�������̬���ʵ��Ȼ�ѧ����ʽ�� ��
��6��Y����ԭ���γ�P4Y3���ӣ��÷�����û�Цм����Ҹ�ԭ���������Ѵ�8���ӽṹ����һ��P4Y3�����к��еļ��Լ��ͷǼ��Լ��ĸ����ֱ�Ϊ ���� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
��12�֣�����ѧ�����л���ѧ������
����������һ�������������˷ܼ�����·�ߺϳ���ͼ��ʾ��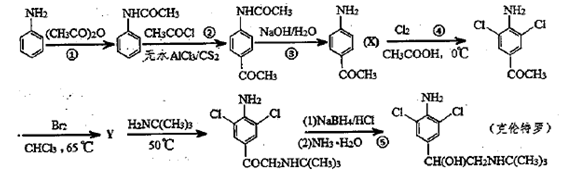
��1���������ķ���ʽΪ ��
��2����Ӧ�ܡ��ݵķ�Ӧ���ͷֱ��� �� ��
��3����Ӧ�۵Ļ�ѧ��Ӧ����ʽΪ ��
��4��Y�Ľṹ��ʽ�� ��
��5�����б����� NHһ���ܷ���������Ӧ��X��ͬ���칹���� �֡�
NHһ���ܷ���������Ӧ��X��ͬ���칹���� �֡�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com