
| A. | ②③④ | B. | ②①④ | C. | ②③① | D. | ②①③ |
分析 酸的概念是根据物质溶于水解离成的阳离子全部为H+来确定的,则在酸的溶液中不会存在金属阳离子,碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;
盐是由金属离子和酸根离子组成的化合物.
解答 解:①Na+不可能是酸电离产生的,酸电离产生的阳离子应全部为H+,为碱、或盐电离,为氢氧化钠或硫酸钠电离;
②因阳离子全部为H+,可理解为盐酸和硫酸两种物质溶于水时电离出的离子;
③Na+、K+不可能是酸电离产生的,因阴离子只有OH-,应为两种碱;
④Na+、K+、NO3-溶液中无H+,不会是酸电离产生的,因有金属离子和硝酸根离子,则为盐电离产生的离子;
按照仅由酸、碱、盐依次电离的是②③④,
故选A.
点评 本题考查了概念的理解和判断,能够从离子的角度来认识酸、碱、盐的概念和构成,并熟悉常见的酸、碱、盐,题目难度不大.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:选择题
| A. | FeCl2、FeCl3 | B. | NaHCO3、Na2CO3 | C. | NaAlO2、AlCl3 | D. | Mg(HCO3)2、MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
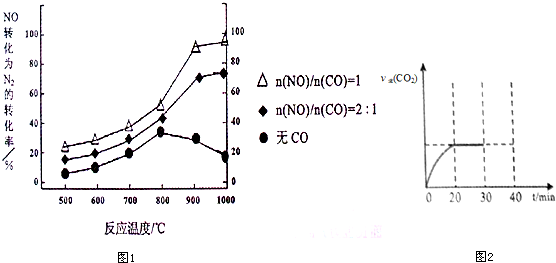
| 浓度/mol?L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
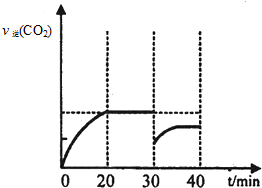 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应中金属共失去电子0.1 mol | |
| B. | 合金中,铜的质量为2.8 g | |
| C. | 原硝酸的浓度:c(HNO3)=4.5 mol•L-1 | |
| D. | 要使溶液中的金属离子完全沉淀,需加5 mol•L-1的NaOH溶液60 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
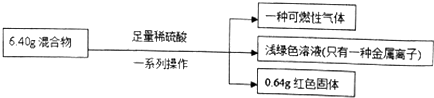
| A. | 原混合物中铜元素的质量一定为0.64g | |
| B. | 生成气体体积为2.016L | |
| C. | 实验中反应的硫酸的物质的量为0.1mol | |
| D. | 原混合物中铁的质量分数为87.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
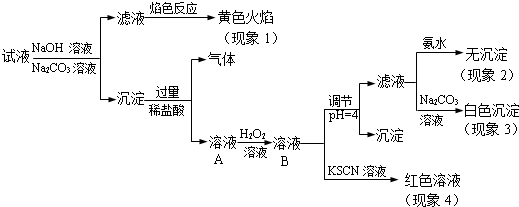
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com