
【题目】实验室以苯甲醛为原料制备间溴苯甲醛,其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。
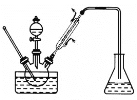
下列说法错误的是( )
A.甲同学认为步骤1中使用1,2-二氯乙烷的目的是作催化剂,加快反应速率
B.乙同学认为可在该实验装置的冷凝管后加接一支装有无水MgSO4的干燥管,实验效果可能会更好
C.丙同学认为步骤2中有机相用10%NaHCO3溶液洗涤可除去大部分未反应的Br2
D.丁同学认为步骤4中减压蒸馏有机相是因为间溴苯甲醛高温下容易氧化或分解
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A.在干冰晶体中,每一个二氧化碳分子周围有12个二氧化碳分子紧密相邻
B.金刚石网状结构中,由共价键构成的碳原子环中,最小的环上有4个碳原子
C.熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
D.在12g金刚石晶体中,含共价键为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是![]()
![]()
A.锅炉中沉积的![]() 可用
可用![]() 溶液浸泡后,再将不溶物用稀盐酸溶解去除
溶液浸泡后,再将不溶物用稀盐酸溶解去除
B.向沸水中滴加![]() 饱和溶液制备
饱和溶液制备![]() 胶体的原理是加热促进了
胶体的原理是加热促进了![]() 水解
水解
C.在室温下,向纯水中加入盐酸或氢氧化钠都能使水电离平衡逆向移动,但是水的离子积不变
D.反应![]() 在一定条件下能自发进行,说明该反应的
在一定条件下能自发进行,说明该反应的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“侯氏制碱法”是我国化工专家候德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程及实验装置(部分夹持装置省略)如下:

下列叙述错误的是
A. 实验时先点燃装置①的酒精灯,过一段时间后再打开装置③中分液漏斗的旋塞
B. 装置②的干燥管中可盛放蘸稀硫酸的脱脂棉,作用是吸收多余的NH3
C. 向步骤Ⅰ所得滤液中通入氨气,加入细小的食盐颗粒并降温,可析出NH4Cl
D. 用装置④加热碳酸氢钠可实现步骤Ⅱ的转化,所得CO2可循环使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的简化核外电子排布式为__,有__个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键,从原子结构角度分析,原因是__。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因__。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | -49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂,Zn、Ge、O电负性由大至小的顺序是__。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为__,微粒之间存在的作用力是___。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为__。
,0)。则D原子的坐标参数为__。
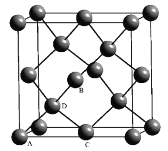

②晶胞参数,描述晶胞的大小和形状。已知单晶Ge的晶胞参数a=565.76pm,其密度为___g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某大型精炼铜厂,在电解铜的阳极泥中含有3-14℅Se元素,(Se和S同主族化学性质相似)以Se单质、Cu2Se存在,还含有稀有金属及贵金属。人体缺乏Se就会得“克山病”,Se也是制光电池的一种原料。从阳极泥中提取Se的流程如下:
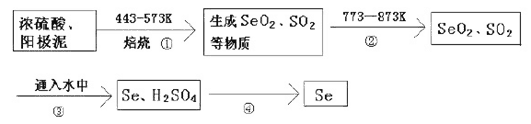
(1)流程②的目的是_________________.流程④操作用到的玻璃仪器有烧杯、______________。
H2SeO3与SO2的离子反应方程式为_____________________________________。
(2)上述工业提取Se的流程中,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是________________。工业提取Se的流程中,可循环利用的物质是_________________。
(3)称取5.000g电解铜阳极泥样品以合适方法溶解,配成250.00mL混酸溶液,移取上述溶液25.00mL于锥形瓶中,加入25.00mL0.01000mol·L-1KMnO4标准溶液{只发生Se(+4)转化为Se(+6)}。反应完全后,用0.05000mol·L-1Fe2+标准溶液滴至终点,消耗15.00mL,则电解铜阳极泥中Se的质量分数为____________。若用FeCl2溶液为Fe2+标准溶液滴至终点,对测定Se的质量分数结果是否有影响,理由是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是
A. 124 g P4含有P—P键的个数为4NA B. 12 g石墨中含有C—C键的个数为1.5NA
C. 12 g金刚石中含有C—C键的个数为4NA D. 60gSiO2中含Si—O键的个数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族化合物A(C9H12O)常用于药物及香料的合成,A有如下转化关系:
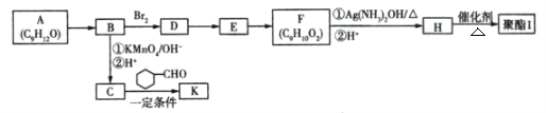
已知:①A的苯环上只有一个支链,支链上有两种不同化学环境的氢原子;
②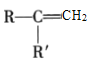
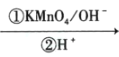
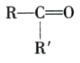 +CO2
+CO2
③![]()
回答下列问题:
(1)A生成B的反应条件为____,由D生成E的反应类型为_________。
(2)F中含有的官能团名称为________。
(3)K中含有两个六元环,则K的结构简式为 ______。
(4)由F生成H过程中①的化学方程式为_______ 。
(5)H有多种同分异构体,写出一种符合下列条件的同分异构体的结构简式 __________。
①能发生银镜反应 ⑦遇FeCl3溶液显色 ③具有4组核磁共振氢谱峰
(6)糠叉丙酮![]() 是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇[ (CH3)3COH]和糠醛
是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇[ (CH3)3COH]和糠醛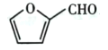 为原料制备糠叉丙酮的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):__________________
为原料制备糠叉丙酮的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它是三原子分子,其摩尔质量为M g·mol--1。NA表示阿伏加德罗常数的数值,则下列说法正确的是( )
A.该气体的物质的量为![]() mol
mol
B.该气体所含原子总数为![]() NA
NA
C.该气体在标准状况下的体积为![]() L
L
D.该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为![]() mol·L-1
mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com