
 TiCl4+2CO
TiCl4+2CO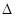 H=-393.5 kJ·mol-1
H=-393.5 kJ·mol-1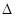 H=-566 kJ·mol-1
H=-566 kJ·mol-1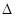 H=+141 kJ·mol-1
H=+141 kJ·mol-1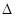 H= ,
H= ,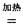 4NaCl+Ti,该反应不能在水溶液中进行,一是因为TiCl4会强烈水解生成TiO2,另一原因 (用适当化学方程式辅以必要的文字说明)。
4NaCl+Ti,该反应不能在水溶液中进行,一是因为TiCl4会强烈水解生成TiO2,另一原因 (用适当化学方程式辅以必要的文字说明)。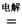 Mg+Cl2 TiCl4+2Mg
Mg+Cl2 TiCl4+2Mg 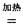 2MgCl2+Ti
2MgCl2+Ti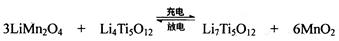 ,使用时先充电,写出其充电式的阳极反应 ,放电时Li+的移动方向 。
,使用时先充电,写出其充电式的阳极反应 ,放电时Li+的移动方向 。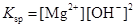 ;氢氧根离子浓度增大,使氢氧化镁的溶解平衡左移,有利于氢氧化镁的析出
;氢氧根离子浓度增大,使氢氧化镁的溶解平衡左移,有利于氢氧化镁的析出 H=(-393.5×2+566+141)kJ·mol-1=-80.0 kJ·mol-1。
H=(-393.5×2+566+141)kJ·mol-1=-80.0 kJ·mol-1。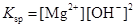 。加入适当过量的熟石灰后,增大量溶液中的氢氧根离子浓度,使溶解平衡向逆反应方向移动,从而有沉淀析出。
。加入适当过量的熟石灰后,增大量溶液中的氢氧根离子浓度,使溶解平衡向逆反应方向移动,从而有沉淀析出。

科目:高中化学 来源:不详 题型:填空题
 CH3OH(g); ΔH1
CH3OH(g); ΔH1 CH3OH(g) +H2O(g);ΔH2
CH3OH(g) +H2O(g);ΔH2| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g);ΔH=-197 kJ·mol-1,当达到化学平衡时,下列说法中正确的是( )
2SO3(g);ΔH=-197 kJ·mol-1,当达到化学平衡时,下列说法中正确的是( )| A.生成SO3 2 mol | B.含氧原子共8 mol |
| C.放出197 kJ热量 | D.SO2和SO3共2 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由2H2(g)+O2(g)=2H2O(l)△H= —571.6 kJ/mol 可知氢气的燃烧热△H= —285.8 kJ/mol |
| B.某离子被沉淀完全是指该离子在溶液中的浓度为0 |
| C.电解精炼铜时以粗铜作阳极 |
| D.对于一个给定的可逆反应,平衡常数只与温度有关,与浓度、压强无关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.当10 NA个电子转移时,该反应放出1300kJ的能量 |
| B.当1 NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C.当2 NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D.当8 NA个碳氧共用电子对生成时,放出1300kJ的能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


| A.负极的电极反应式为: CO+O2—―2e-=CO2 |
| B.工作时电极b作正极,O2-由电极a流向电极b |
| C.工作时电子由电极a通过传感器流向电极b |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3 (g) △H =-196.6kJ·mol-1
2SO3 (g) △H =-196.6kJ·mol-1 2NO2 (g) △H =-113.0kJ·mol-1
2NO2 (g) △H =-113.0kJ·mol-1 SO3 (g) +NO(g)的△H =______kJ·mol-1
SO3 (g) +NO(g)的△H =______kJ·mol-1 CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H _____0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,
CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H _____0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.488.3 kJ·mol-1 | B.-244.15 kJ·mol-1 |
| C.244.15 kJ·mol-1 | D.-488.3 kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com