


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:阅读理解
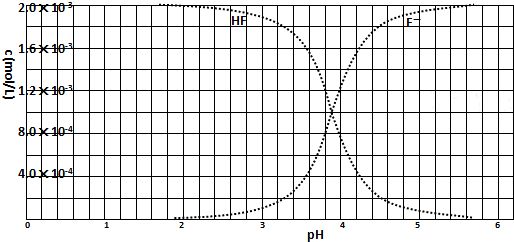
 (2010?浙江)已知:
(2010?浙江)已知:
| c(H+)?c(F-) |
| c(HF) |
| c(H+)?c(F-) |
| c(HF) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高二化学(上) 题型:013
用20mL 0.05mol·L-1 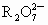 离子的溶液恰好能将20mL 0.3mol·L-1的Fe2+溶液完全氧化,则元素R在还原产物中的化合价为
离子的溶液恰好能将20mL 0.3mol·L-1的Fe2+溶液完全氧化,则元素R在还原产物中的化合价为
[ ]
|
A.+2 |
B.+3 |
|
C.+4 |
D.+5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com