
【题目】实验室欲用NaOH固体配制0.1mol/L的NaOH溶液480mL:
(1)配制溶液时,一般可以分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动。其正确的操作顺序为______________(填选项)
A. ②①③⑧⑤⑥⑦④⑨ B. ②①③⑧⑤⑥⑨⑦④ C. ②①⑨③⑧⑤⑥⑦④
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、_________、__________。
(3)计算所需NaOH的质量为_________。
(4)容量瓶使用前必须___________,容量瓶上需标有__________
(5)在配置过程中,其他操作都正确,下列操作会引起浓度偏高的是_________。
A. 转移溶液时不慎有少量洒到容量瓶外面
B. 定容时俯视刻度线
C. 未冷却到室温就将溶液转移到容量瓶并定容
D. 定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
【答案】B 500mL容量瓶 胶头滴管 2g 检验是否漏液 温度、容量、刻度线 BC
【解析】
(1)配制一定物质的量浓度溶液,其一般步骤:计算;称量(量取);溶解;冷却;转移;洗涤;摇动;定容;摇匀;装瓶、贴标签。所以正确操作顺序为②①③⑧⑤⑥⑨⑦④,选B,故答案为:B。
(2)配制一定物质的量浓度溶液,用到的仪器有天平(量筒)、药匙、玻璃棒、烧杯、一定规格的容量瓶、胶头滴管,故答案为:
500mL容量瓶;胶头滴管;
(3)0.1mol/L 500mLNaOH溶液的物质的量为![]() ,其质量为
,其质量为![]() ,故答案为:2g;
,故答案为:2g;
(4)容量瓶使用前必须检验是否漏液,容量瓶上需标有温度、容量、刻度线,故答案为:检验是否漏液;温度、容量、刻度线;
(5)A. 转移溶液时不慎有少量洒到容量瓶外面,导致溶质的物质的量偏小,所配溶液的浓度偏低,不选A;
B. 定容时俯视刻度线,导致溶液的体积偏小,配溶液的浓度偏高,选B;
C. 未冷却到室温就将溶液转移到容量瓶并定容,导致溶液的体积偏小,配溶液的浓度偏高,选C;
D. 定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致溶液的体积偏大,所配溶液的浓度偏低,不选D;故答案为:BC。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】阿司匹林口服时,具有解热镇痛作用。是一种常用的治疗感冒的药物,也可用于抗风湿,促进痛风患者尿酸的排泄。近年来还发现阿司匹林能抑制血小板凝聚,可防止血栓的生成。它的有效成分是乙酰水杨酸( )。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐【(CH3CO)2O】为主要原料合成乙酰水杨酸。
)。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐【(CH3CO)2O】为主要原料合成乙酰水杨酸。
【反应原理及部分装置】

【实验流程】

已知:①醋酸酐遇水分解生成醋酸。
②水杨酸和乙酰水杨酸均微溶于水,但其钠盐易溶于水,副产物为高分子化合物,难溶于水。
回答下列问题:
(1)合成过程中要控制温度在85℃~90℃,最合适的加热方法 。
(2)用图1装置过滤比普通漏斗过滤的优点是 。
(3)粗产品提纯:
①分批用少量饱和NaHCO3溶液溶解粗产品,目的是 ;判断该过程结束的现象是 。
②加浓盐酸、冷却后的操作是__________、______、干燥、称重、计算产率。
③纯度检验:取少许产品加入盛有2 mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色。可能的原因是 。
(4)阿司匹林药片中乙酰水杨酸含量的测定步骤(假定只含乙酰水杨酸和辅料,辅料不参与反应):
Ⅰ.称取阿司匹林样品mg;
Ⅱ.将样品研碎,溶于V1 mL a mol/LNaOH(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;
Ⅲ.向锥形瓶中滴加几滴甲基橙,用浓度为b mol/L的标准盐酸滴定剩余的NaOH,消耗盐酸的体积为V2 mL。
已知:乙酰水杨酸与过量NaOH溶液加热发生反应的化学方程式:

则阿司匹林药片中乙酰水杨酸质量分数的表达式为:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图1表示0.001 mol·L-1盐酸滴定0.001 mol·L-1 NaOH溶液的滴定曲线
B. 图2表示从能量角度考虑,石墨比金刚石稳定
C. 图3表示Al3+与OH-反应时含铝微粒浓度变化曲线,图中a点溶液中含大量Al3+
D. 图4所示图中的阴影部分面积的含义是(v正-v逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.强酸、强碱、重金属盐等可使蛋白质变性
B.用新制氢氧化铜悬浊液(必要时可加热)能鉴别甲酸、乙醇、乙醛
C.乙酸乙酯中混有的乙酸,可加入足量的饱和![]() 溶液,经分液除去
溶液,经分液除去
D.向苯和苯酚的混合液中加入浓溴水,充分反应后过滤,可除去苯中少量的苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用ClCH2CH2PO(OH)2(乙烯利![]() 及Br2/CCl4(CCl4的沸点为76.8℃)等为原料制备1,2-二溴乙烷
及Br2/CCl4(CCl4的沸点为76.8℃)等为原料制备1,2-二溴乙烷![]() 沸点为131,4℃)的装置如图所示。已知a中发生的反应为ClCH2CH2PO(OH)2+4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O。下列说法错误的是( )
沸点为131,4℃)的装置如图所示。已知a中发生的反应为ClCH2CH2PO(OH)2+4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O。下列说法错误的是( )
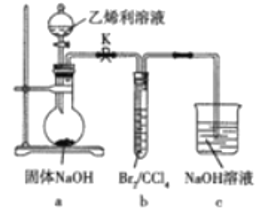
A.向圆底烧瓶中滴加乙烯利溶液前需先打开K
B.实验过程中装置b中的液体逐渐变为无色
C.装置c中的NaOH溶液的作用是吸收挥发出的Br2和乙烯
D.装置b中反应后的混合液经Na2SO3溶液洗涤、水洗、干燥、蒸馏得1,2-二溴乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2-二溴乙烷,装置如下图所示:
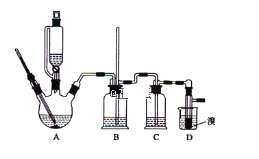
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)写出由乙醇制备乙烯的化学方程式______________________________,乙烯制备1,2-二溴乙烷的化学方程式_______________________________。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___________;(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置A中除了浓硫酸和乙醇外,还应加入_____,其目的是_______装置A中生成副产物乙醚的化学反应方程式 ___________________。
(4)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放 ________________,
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液d.品红和酸性KMnO4
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____层(填“上”、“下”);若产物中有少量副产物乙醚。可用_______的方法除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法错误的是
)是最简单的一种。下列关于该化合物的说法错误的是
A. 与环戊烯互为同分异构体
B. 二氯代物超过两种
C. 所有碳原子均处同一平面
D. 生成1 molC5H12至少需要2 molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是同周期主族元素,Y的最外层电子数是X次外层电子数的3倍,四种元素与锂组成的盐是一种新型的锂离子电池的电解质(结构如图,箭头指向表示共同电子对由W提供)。下列说法不正确的是( )
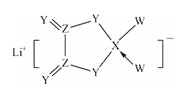
A.W的非金属性比Y的强 B.在该物质中Ⅹ原子满足8电子稳定结构
C.该物质中含离子键和共价键 D.Z的氧化物都易溶于水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向温度为300℃的2L密闭容器中充入2molSO2和1molO2发生反应:![]() ,体系达到平衡状态后SO2的浓度为0.1mol/L,下列说法错误的是
,体系达到平衡状态后SO2的浓度为0.1mol/L,下列说法错误的是
A. 该温度下反应的平衡常数K=1620
B. SO2和O2的平衡转化率相等
C. 平衡后保持温度和容器体积不变再充入SO3(g),平衡逆向移动且平衡常数不变
D. 若不再向容器中加入任何物质,改变条件不可能使SO2的浓度达到1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com