
【题目】Cu(OH)2在水中存在着如下溶解平衡:Cu(OH)2 (s)Cu2+(aq)+2OH﹣ (aq),在常温下Ksp[Cu(OH)2]=2×10﹣20 . 某CuSO4溶液中,c(Cu2+)=0.02molL﹣1 , 在常温下要生成Cu(OH)2沉淀,需要向CuSO4溶液中加入碱溶液来调节溶液的pH,使溶液的pH大于( )
A.2
B.3
C.4
D.5
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是( )
A.H+、Fe2+、NO3-、Cl-B.S-、Na+、H+、K+
C.K+、CO32-、Br-、AlO2-D.H+、Cl-、Na+、S2O32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)稀硫酸跟氧化镁反应(写出离子方程式)
(2)盐酸跟碳酸氢钠溶液反应(写出离子方程式)
(3)Cu2++2OH﹣=Cu(OH)2↓(写出化学方程式)
(4)氢氧化铁胶体制备(写出化学方程式) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:归纳正确的是( ) ①向0.1molL﹣1 CH3COOH溶液中加入少量冰醋酸,平衡向正反应方向移动,电离程度增大;②常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c(Na+)+c(H+)=c(OH﹣)+c(CH3COO﹣)
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同;④常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;则有:KaKh=Kw .
A.①②④
B.②④
C.②③
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫﹣氨热化学循环制氢示意图如下: 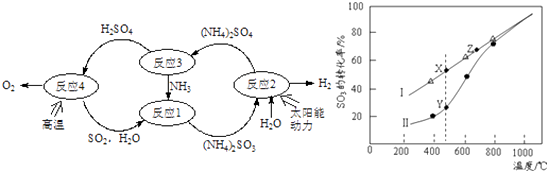
(1)反应1的离子方程式为 .
(2)反应2能量转化主要方式为 .
(3)反应3中控制反应条件很重要,不同条件下硫酸铵分解产物不同.若在400℃时分解,产物除水蒸气外还有A、B、C三种气体,A是空气中含量最多的单质,B能使湿润的红色石蕊试纸变蓝,C能使品红溶液褪色.则400℃时硫酸铵分解的化学方程式为 .
(4)反应4是由(a)、(b)两步反应组成:
H2SO4(l)=SO3(g)+H2O(g),△H=+177kJmol﹣1…(a)
2SO3(g)2SO2(g)+O2(g),△H=+196kJmol﹣1…(b)
①则H2SO4(l)分解为SO2(g)、O2(g)及H2O(g)的热化学方程式为: .
②在恒温密闭容器中,控制不同温度进行SO3分解实验.以SO3起始浓度均为cmolL﹣1 , 测定SO3的转化率,结果如图2,图中Ⅰ曲线为SO3的平衡转化率与温度的关系,Ⅱ曲线表示不同温度下反应经过相同反应时间且未达到化学平衡时SO3的转化率.
(i)图中点X与点Z的平衡常数K:
K(X)K(Z)(选填:>,<,=);
(ii)Y点对应温度下的反应速率:
v(正)v(逆)(选填:>,<,=);
(iii)随温度的升高,Ⅱ曲线逼近Ⅰ曲线的原因是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质。回答下列问题:

(1)写出各物质的化学式:A.___,B.___,C.____,D.____,E.____。
(2)写出B→C、D→E反应的离子方程式:
B→C:____________________________________________________________;
D→E:____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空
(1)按系统命名法命名:
①  ,写出它和氯气发生一取代反应的方程式
,写出它和氯气发生一取代反应的方程式
②  ;它的一氯代物具有不同沸点的产物有 种
;它的一氯代物具有不同沸点的产物有 种
(2)写出下列各有机物的结构简式:
①2,3﹣二甲基﹣4﹣乙基已烷: ;
②支链只有一个乙基且相对分子质量最小的烷烃: ;
(3)羟基的电子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有关实验寧实的说明或解释正确的是
A. 用坩埚钳夹住一小块用砂纸打磨过的铝箔在洒精灯上加热,铝熔化但不滴落,说明Al2O3的熔点高于Al
B. 向某溶液中先淌加Ba(NO3)2溶液,出现白色沉淀,再滴加稀硝酸,沉淀不溶解,说明原溶液中一定含有SO42-
C. 向新制氯水中加入少量NaHCO3固体,出现较多气体,说明HClO的酸性强于H2CO3
D. 向某溶液中先滴加KSCN溶液,溶液不变红,再滴加双氧水,溶液变红,说明原溶液中一定含有Fe2+
【答案】AD
【解析】A、加热打磨过后的铝箔,铝表面生成氧化铝薄膜,铝熔化说明铝熔点低,但铝不滴落,说明氧化铝熔点非常高,故A正确;B、溶液中也可能存在的SO32-,Ba2+与SO32-反应生成白色的BaSO3沉淀,SO32-有强还原性,再加硝酸,硝酸将BaSO3氧化为不溶于硝酸的BaSO4,所以无法判断原溶液中是否含有SO42-,故B错误;C、氯气与水反应生成盐酸和次氯酸,加入NaHCO3固体,产生CO2,只能说明氯水酸性强于H2CO3,并不能说明HClO酸性强于碳酸,故C错误;D、向溶液中先滴加KSCN溶液,溶液不变红,则证明溶液中不含Fe3+,再加双氧水,溶液变红,说明原溶液中一定含有Fe2+被双氧水氧化为Fe3+,故D正确。故选AD。
【题型】多选题
【结束】
21
【题目】某种制取纯碱的方法如下:
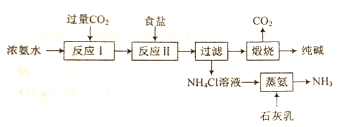
(1)写出“反应I ”的化学方程式:__。
(2)“反应Ⅱ”为复分解反应,反应中所涉及物质的溶解度如图所示。写出“反应Ⅱ”的化学方程式:__。

(3)写出“煅烧”反应的化学方程式:__。
(4) “蒸氨”时需要加热,写出“蒸氨”时反应的化学方程式:___。
(5)写出将“蒸氨”产生的氨气通入Al2(SO4)3溶液中时反应的离子方程式: __。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com