
����Ŀ����t��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10��10 �� ����˵������ȷ���ǣ� �� 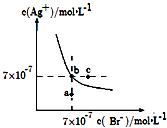
A.��ͼ��a���Ӧ����AgBr�IJ�������Һ
B.��t��ʱ��Ksp��AgBr��=4.9��10��13
C.��t��ʱ��AgCl��s��+Br����aq��AgBr��s��+Cl����aq����ƽ�ⳣ��K��816
D.��AgBr�ı�����Һ�м���NaBr���壬��ʹ��Һ��b�㵽��c��
���𰸡�D
���������⣺A������ͼ���֪����a��ʱQc=c��Ag+��c��Br������Ksp������a��ΪAgBr�IJ�������Һ����A��ȷ��
B�����ͼ��c���c��Ag+����c��Br������֪�����¶���AgBr��Ksp=7��10��7��7��10��7=4.9��10��13 �� ��B��ȷ��
C����ӦAgCl��s��+Br����aq��AgBr��s��+Cl����aq����ƽ�ⳣ��Ϊ��K= ![]() =
= ![]() =
= ![]() ��816����C��ȷ��
��816����C��ȷ��
D����AgBr������Һ�м���NaBr�����c��Br���������ܽ�ƽ�������ƶ���c��Ag+����С����D����
��ѡD��
A����a��ʱQc=c��Ag+��c��Br������Ksp���ж�AgBrΪ��������Һ��
B������ͼ��c���c��Ag+����c��Br�����ɵø��¶���AgBr��KspΪ4.9��10��13��
C������K= ![]() =
= ![]() �����ƽ�ⳣ�����ɣ�
�����ƽ�ⳣ�����ɣ�
D����AgBr������Һ�м���NaBr�����c��Br���������ܽ�ƽ�������ƶ���c��Ag+����С��


 Сѧ��ĩ���100��ϵ�д�
Сѧ��ĩ���100��ϵ�д� ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС�����ʵ��̽����Ӧ���ʵIJⶨ�ͱȽϡ�
��ʵ��Ŀ�ġ��ⶨп��ϡ���ᷴӦ������
��ʵ����Ʒ����ƿ��˫��������Ƥ�ܡ���Һ©����ֱ�ǵ��ܡ�50mLע����������̨�������п����1 mol/L���ᡢ4 mol/L���ᡣ
��ʵ�鲽�衿
��1��ȡһ��װ��(��ͼ��ʾ)������40 mL 1 mol/L�������п���������ռ�10 mL H2�����ʱ�䡣
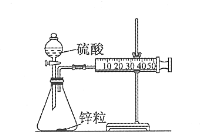
��2��ȡ��һ��װ�ã�����40 mL4 mol/L�������п���������ռ�10 mL H2�����ʱ�䡣
��ʵ������п��ϡ���ᷴӦ ��д�������ռ�10mL���壬��2������ʱ��ȣ�1������ʱ��_________��
��ʵ������
�����Լ� | ��Ӧʱ�� | ��Ӧ���� |
40 mL 1 mol/L���� | �� | _________ |
40 mL 4 mol/L���� | �� | _________ |
��ʵ����ۡ�4 mol/L������п��Ӧ��1 mol/L������п��Ӧ������ ��
��ע�������1��п�Ŀ���(�������)��С ��
��2��40 mL������ҪѸ�ټ��룻
��3��װ�� ���Ҽ�ʱҪѸ��ȷ��
��4�������ռ���������ˮ����װ��(��ͼ��ʾ)���档
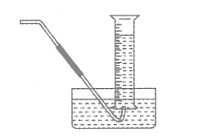
��ʵ�����ۡ�����ʵ��ⶨ��Ӧ���ʵķ����⣬���еķ�������(����������)��
��1�� ��
��2�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ�����������������Һ�п�����UO22+��U2O72-��ʽ���ڣ���Ҫ��д��UO3��ǿ�ᡢǿ�Ӧ�����ӷ���ʽ��
��1��______________________________����2��_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ����( )
A. NH3��CO��CO2���Ǽ��Է���
B. CH4��CCl4���Ǻ��м��Լ��ķǼ��Է���
C. HF��HCl��HBr��HI���ȶ���������ǿ
D. CS2��H2O��C2H2����ֱ���η���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ�������¾��ܲ����������������ʺ������Ա(�Ա���������������Ҫ����̫�շ��еĺ������)����ʱ�Ĺ��������� (����)
A.H2O2B.KMnO4
C.KClO3D.Na2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ƚ����и����Ȼ�ѧ����ʽ�Ц�H�Ĵ�С��ϵ��
(1)S(s)��O2(g)===SO2(g) ��H1
S(g)��O2(g)===SO2(g) ��H2
��H1__________��H2
(2)CH4(g)��2O2(g)===CO2(g)��2H2O(l) ��H1
CH4(g)��2O2(g)===CO2(g)��2H2O(g) ��H2
��H1__________��H2
(3)4Al(s)��3O2(g)===2Al2O3(s) ��H1
4Fe(s)��3O2(g)===2Fe2O3(s) ��H2
��H1__________��H2
(4)ú��Ϊȼ����2��;����
;��1����ֱ��ȼ�գ�
C(s)��O2(g)===CO2(g) ��H1<0
;��2��������ˮú����
C(s)��H2O(g)===CO(g)��H2(g) ��H2>0
��ȼ��ˮú����
2CO(g)��O2(g)===2CO2(g) ��H3<0
2H2(g)��O2(g)===2H2O(g) ��H4<0
��H1����H2����H3����H4�Ĺ�ϵʽ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A������ʳƷ��ҵ����֪9.0g A������O2�г��ȼ�գ������ɵĻ����������ͨ��������Ũ����ͼ�ʯ�ң��ֱ�����5.4g��13.2g��������ʣ������ΪO2 ��
��1��A���ӵ�����ͼ��ͼ��ʾ����ͼ�п�֪����Է��������� �� ��A�ķ���ʽ���� 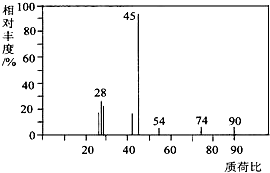
��2��A����NaHCO3��Һ������Ӧ��Aһ�����еĹ���������
��3��A���ӵĺ˴Ź���������4�����շ壬�����֮����1��1��1��3����A�Ľṹ��ʽ��
��4����д����������A��ͬ��ͬ���칹��Ľṹ��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п�̸ɵ�����й�������ȣ���������뻷�����������Σ����ij��ѧ��ȤС����������´����������շϵ���еĸ�����Դ 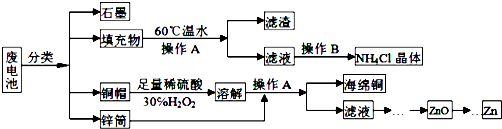
��1��ͭñ�ܽ�ʱ����H2O2��Ŀ�������û�ѧ����ʽ��ʾ����
��2����������Ҫ�ɷ�Ϊ���̻������̻�����м���һ������ϡ���ᡢϡ���ᣬ�����Ͻ�����������Ϊֹ����Ҫ��ӦΪ��2MnO��OH��+MnO2+2H2C2O4+3H2SO4�T3MnSO4+4CO2��+6H2O��
�ٵ�1mol MnO2�μӷ�Ӧʱ������mol ���ӷ���ת�ƣ�
��MnO��OH����Ũ�����ڼ���������Ҳ�ɷ�����Ӧ����д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3������п�̸ɵ�صĵ����ΪKOH��Һ����֪���ܷ�Ӧ����ʽΪ��
Zn+2MnO2+2H2O�T3MnOOH+Zn��OH��2 �� �为���缫��ӦʽΪ ��
��4��ZnO ��Al2O3�Ļ�ѧ�������ƣ�д��ZnO��NaOH��Һ��Ӧ�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com