
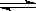 H++OH- NH3+H2O
H++OH- NH3+H2O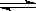 NH3·H2O
NH3·H2O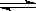 NH3·H2O + H+ NH3·H2O
NH3·H2O + H+ NH3·H2O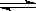 NH4+ +OH-
NH4+ +OH-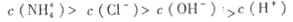
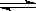 NH3·HDO + DCl
NH3·HDO + DCl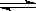 H++OH-、NH3+H2O
H++OH-、NH3+H2O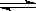 NH3·H2O、NH4+ + H2O
NH3·H2O、NH4+ + H2O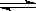 NH3·H2O + H+、NH3·H2O
NH3·H2O + H+、NH3·H2O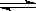 NH4+ +OH-;溶液呈碱性,说明氨水的电离程度大于氯化铵的水解程度,因此关系式为
NH4+ +OH-;溶液呈碱性,说明氨水的电离程度大于氯化铵的水解程度,因此关系式为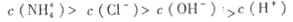 。
。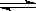 NH3·HDO + DCl。
NH3·HDO + DCl。

科目:高中化学 来源:不详 题型:推断题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
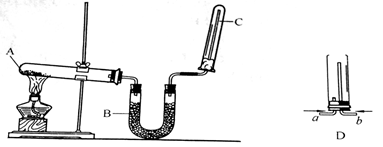
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.1∶1∶3 | B.1∶2∶4 | C.1∶1∶4 | D.1∶3∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
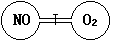
| A.减小 | B.增大 | C.不变 | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.30% | B.70% | C.63% | D.84% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
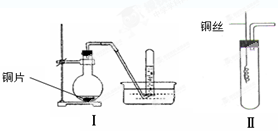
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.亚硝酸钠可作防腐剂,所以没毒 |
| B.可用淀粉KI溶液来鉴别亚硝酸钠和氯化钠 |
| C.亚硝酸银和氯化银都是白色沉淀,不能用硝酸银和稀硝酸来鉴别亚硝酸钠与氯化钠 |
| D.氯化钠为白色固体,亚硝酸钠为红棕色固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com