
【题目】对于平衡体系:mA(g)+ nB(g)![]() pC(g)+ qD(g),下列判断正确的是( )
pC(g)+ qD(g),下列判断正确的是( )
A.若温度不变将容器的容积增大1倍,达到新平衡时A的浓度变为原来的0.55 倍,则m+n<p+q
B.若升高平衡体系的温度,达到新平衡时A 的浓度变为原来的0.55 倍,说明该反应△ H<0
C.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
D.若平衡后同时增大A、B的浓度,则A、B的转化率一定都减小
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列操作中正确的是 ( )
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部。
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种元素,A、B同周期,A、B可形成两种无色无味气体AB和AB2。D在B的下一周期,其最高价氧化物的水化物是二元强酸,D、C可形成离子化合物CD,D离子比C离子多一个电子层。据此可知:
(1)这四种元素分别是A:______、B:_____、C:_____、D:_____。
(2)C离子的离子结构示意图是____________________。
(3)化合物CD的电子式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有①Na+ 、②Ba2 +、③Cl一、④Br一、⑤SO32一、⑥SO42一 离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下。

下列结论正确的是( )
A. 肯定含有的离子是①④⑤ B. 肯定没有的离子是②⑥
C. 不能确定的离子是① D. 不能确定的离子是③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.自发反应的熵一定增大,非自发反应的焓一定减小
C.对于熵增反应,若一定温度下不能自发进行,则该反应的△H>0
D.对于△H >0的反应能自发进行,则该反应的△S<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法不正确的是
A. 乙烯可作水果的催熟剂
B. 硅胶可作袋装食品的干燥剂,铁粉可做脱氧剂
C. 福尔马林可作食品的保鲜剂
D. 氢氧化铝可作胃酸的中和剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种原子序数增大的元素,只有一种为金属。A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满。
(1)E元素的名称为________,该元素基态原子的价电子排布式为_______。
(2)B与D分别与氢形成最简单氢化物沸点高低顺序为____(用化学式表示);原因_____。
(3)A、B、C三种元素分别与氢形成化合物中的M-M(M代表A、B、C)单键的键能如下表:

上述三种氢化物中,A、B、C元素原子的杂化方式有_____种;请解释上表中三种氢化物M-M单键的键能依次下降的原因______________________。
(4)D与氯形成的化合物DC15,加压条件下148℃液化,发生完全电离得到一种能够导电的熔体,测定D-Cl键长为198pm和206pm两种,该熔体中含有一种正四面体结构的阳离子,请写出该条件下DC15电离的电离方程式__________;该熔体中阴离子的空间构型为________。
(5)E与C形成的化合物晶体结构有四种,其中一种与金刚石类似,金刚石晶体结构如图所示,该晶体的化学式为______(用元素符号表示);该晶胞的棱长为apm 则该晶体的密度为______g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2 L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
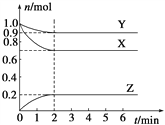
(1)该反应的化学方程式为_______________。
(2)反应开始至2 min,气体Z的反应速率为____________。
(3)若X、Y、Z均为气体,反应达到平衡时,压强是开始时的________倍;此时放出了a kJ的热量,则按(1)的反应方程式写成热化学反应方程式时,该反应的反应热ΔH=_____________。
(4)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。已知:
化学键 | H—H | H—Cl | Cl—Cl |
键能/ kJ·mol–1 | 436 | 431 | 242 |
工业上通过氢气在氯气中充分燃烧制取HCl气体,写出该反应的热化学反应方程式:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com