
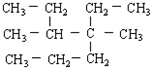
 的正确系统命名为
的正确系统命名为 ,故答案为:
,故答案为: ;
; 的名称为:3,4-二甲基-4-乙基庚烷,
的名称为:3,4-二甲基-4-乙基庚烷,

 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
| A、元素周期表中一共有18个纵行 |
| B、原子最外层电子数为2的元素全部位于周期表的第ⅡA族和零族 |
| C、同周期第ⅡA族与第ⅢA族元素的原子序数之差可能为25 |
| D、同主族两种元素的原子序数之差可能为44 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合物(括号内为杂质) | 除杂试剂(填序号) | 反应离子方程式 |
| ①FeCl3(FeCl2) | ||
| ②Mg(Al) | ||
| ③NaBr(NaI) | ||
| ④SiO2 (CaCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(HCO3-) |
| c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠 |
| B、“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液 |
| C、最后变成的白色固体粉末是碳酸钠 |
| D、该过程的所有化学反应均为化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体一定是混合物 |
| B、胶体与溶液的本质区别是有丁达尔效应 |
| C、将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D、胶体稳定的原因是因为胶体带电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com