
����Ŀ�����淴Ӧ��X(g)+2Y(g)![]() 2Z(g)��2M(g)
2Z(g)��2M(g)![]() N(g)+P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܱո��塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ���������෴Ӧ���¶���ͬ���������ж���ȷ���ǣ�
N(g)+P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܱո��塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ���������෴Ӧ���¶���ͬ���������ж���ȷ���ǣ�

A����Ӧ�ٵ�����Ӧ�����ȷ�Ӧ
B����ƽ�⣨I��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ14:15
C����ƽ�⣨I��ʱX��ת����Ϊ5/11
D����ƽ�⣨I����ƽ�⣨II����M�����������ͬ
���𰸡�C
��������
��������� A����������ƽ�⣨����ƽ�⣨���ƶ���ͬʱX��Y��Z�������ʵ������٣�˵��ƽ�������ƶ�������Ӧ���ȣ�A��������B��ƽ��ʱ���ұ����ʵ������䣬��ͼ���Կ�����ƽ�⣨��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ��2��2.2��10��11��B�����C����ƽ�⣨��ʱ���ұ���������ʵ������䣬��Ϊ2mol����������ѹǿ��ȣ���ƽ��ʱ�����������ʵ���Ϊxmol�����У�2��x=2.2��2.8�����x=28/11mol�������ʵ���������3mol��28/11mol��5/11mol�����Դ�ƽ�⣨��ʱ��X��ת����Ϊ5/11��C����ȷ��D����ƽ�⣨��ƽ�⣨����ѧ��Ӧ�ڷ����ƶ���M���������������ȵ���D�����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��2����ѧ�뼼��]
�����ǹ�ҵ��������Ҫ�IJ�Ʒ֮һ���ںܶ���������Ҫ��;���ش��������⣺
��1�������Ṥҵ�����У��ҹ����û�����Ϊԭ������SO2����Ӧ�Ļ�ѧ����ʽΪ_________________���÷�Ӧ��___________________(���豸����)�н��С�
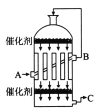
��2��Ϊ��������SO2ת��ΪSO3�����ܳ���������ܣ��ɲ������ж����������Ƚ�������______(���豸����)�н��з�Ӧ������ͼ��ʾ��װ���У�C��������������_______(���豸����)����______���գ��õ�Ũ����������ᡣ
��3��ʵ���ã�SO2����SO3��ת�������¶ȡ�ѹǿ�Ĺ�ϵ���±���ʾ����֪400��600�������Ĵ�Ч���Ϻã��������ʵ�ʣ�ѡ������ʵ�����������___________��

��4�������SO2�ķ�Ӧ���ʺ�ת���ʣ����д�ʩ���е���__________(��ѡ����ĸ)��
A����װ����ͨ�뵪���ұ���������� B����װ����ͨ���Թ��������ұ����������
C�����Ӹ���Ĵ��� D�������¶ȣ���ʱת��SO3
��5���������ų���β���У���SO2�ĺ�������500![]() L��L-1����Ҫ���Դ�������������֮һ���ð�ˮϴ������������������ˮ����β����SO2�Ļ�ѧ����ʽΪ__________________________________��
L��L-1����Ҫ���Դ�������������֮һ���ð�ˮϴ������������������ˮ����β����SO2�Ļ�ѧ����ʽΪ__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϊ����ѧ�����ѡ��1����ѡ���⣬
��һ����������Ѽ������������������Ѽ�ײ͵IJ���ԭ�����£��� Ѽ�⡢�� ��ۡ��� �ƹϡ��� ʳ�Ρ���ش�
��1���������۵��� ������ţ���ͬ������2�����������ʵ��� ��
��3������ά���ص��� �� ��4�����ڵ�ζ������ ��
��������������������������ͷ�չ����Ҫ���ʻ�����
��1���Թܡ��ձ�����ƿ�Ȼ�ѧ��������Ҫ������ ��
A������ B���մ�
��2��������Ŀǰ�����������Ͻ𡣸����Ӵ���ˮ�����绯ѧ��ʴ���为����ӦʽΪ ��
A��O2+2H2O + 4e- = 4OH- B��Fe - 2e -= Fe2+
������������ˮ��Ҫ��Դ���ȼҵ�����Ϲ�ҵ��δ�����������ŷš�ij�������Է�ˮ����Ҫ��Hg2+��H+��Na+��Cl���ȣ��Ĵ���������������ͼ��ʾ��
 ��ش�
��ش�
��1��������ˮδ������ֱ���ŷŵ�Σ���� ������ĸ����
a. ���ˮ����Ⱦ b. ���������ж�
��2�����ڷ�ˮpHʱ�������ҺA������ ������ĸ����
a. ���� b. NaOH��Һ
��3��Na2S��Hg2+������Ӧ�����ӷ���ʽ�� ��
��4���÷�ˮ����������й��������£��������Ӻ��Բ��ƣ���
���� | Na+ | Fe2+ | Cl�� | SO42�� |
Ũ�ȣ�mol/L�� | 3.0��10-4 | 2.0��10-4 | 2.5��10-4 |
��c(Fe2+) = mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2010�괺��2013���������귢��������ʡ�����غ���ǣ����ȫ��������ģ��������Ƕ�ˮ��Դ���ٴ����ӡ�ˮ��������������Ҫ��ѧ���ʣ��й�ˮ�ķ�Ӧ�кܶࡣ
��1���õ���ʽ��ʾH2O���γɹ��� ��
��2����pH=1��ˮ��Һ�У���NH4+��Al3+��Br-��SO42- �� Na+��Fe2+��Cl-��NO3-
��K+��Ba2+��Cl-��NO3- ��K+��Na+��HCO3-��SO42-���������У�һ������������� (�����)��
��3�������з�Ӧ�У�ˮ�������������� (����ĸ����ͬ)��ˮ�Ȳ����������ֲ�����ԭ������ ��
A��2F2��2H2O��4HF��O2 B��2Na2O2��2H2O��4NaOH��O2��
C��CaH2��2H2O��Ca(OH)2��2H2�� D��3Fe��4H2O![]() Fe3O4��4H2]
Fe3O4��4H2]
��4���������ߺš��ɴ��ϵ�������Ҫ������̫���ܺ�ȼ�ϵ�أ�H2��O2��KOH��ˮ��Һ���γ�����ȼ�ϵ�أ������ĵ缫��ӦΪ ����Ӧ������ˮ�����������Ϊ����Ա������ˮ�����õ�1.8 L����ˮʱ�������ת�Ƶĵ�����ԼΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ͭ��ˮ�Ĺ���������м���Ӧ��DZ�ܣ��Ǽ��߿���ǰ������ɫ�����������Ŀǰ��Ҫ�ĺϳɷ����е�ⷨ�����¹��෨�ȡ�
��1�����о����������������ɹ��Ƶ���Cu2O ����������װ����ͼ��
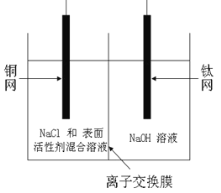
�õ�ص�������Ӧ����ʽΪ ���ӽ���ĤΪ_______(��������)���ӽ���Ĥ��ͭ��Ӧ���ӵ�Դ��_____����
��2���ڸ������ü��齫��״CuO ��ԭҲ���Ƶ�Cu2O��
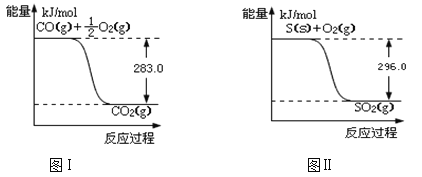
��֪����2Cu(s)��1/2O2(g)=Cu2O(s)����H = -169kJ/mol
��CH4(g)��2O2(g)=CO2(g)+2H2O(g)����H = -846.3 kJ/mol
�� Cu(s)��1/2O2(g)=CuO(s)����H = -157 kJ/mol
��÷�Ӧ���Ȼ�ѧ����ʽ�ǣ�__________��
��3������ͬ���ܱ������У��õ���������������Cu2O(�ò�ͬ�����Ƶ�)�ֱ���д��ֽ�ˮ��ʵ�飺2H2O(g) ![]() 2H2(g)+O2(g) ��H>0��ˮ����Ũ����ʱ��t�仯���±���ʾ��
2H2(g)+O2(g) ��H>0��ˮ����Ũ����ʱ��t�仯���±���ʾ��
��� |
| 0 | 10 | 20 | 30 | 40 | 50 |
�� | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
�� | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
�� | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
�ٶԱ�ʵ����¶ȣ�T2 T1(���������������)��ԭ����___________________��
��ʵ���ǰ20 min��ƽ����Ӧ���� v(O2)=
�۱Ƚϲ�ͬ�����Ƶõ�Cu2O�Ĵ�Ч��Ӧѡ��__________��ʵ�飬ԭ����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����̼��һ����;�㷺�Ļ�������ԭ�ϡ��л�����ⷴӦ�����dz��õĴ�������H2��һ�㺬����CO��ʹ�������ж�������Ӧ����������CO������������Ͷ������SO2��ΪŪ��÷����Դ�����Ӱ�죬����������£�
�ش��������⣺
��1��SO2(g) + 2CO(g) ![]() S(s) + 2CO2(g) ��H �� ���÷�Ӧ��ƽ�ⳣ���ı���ʽ�� ��
S(s) + 2CO2(g) ��H �� ���÷�Ӧ��ƽ�ⳣ���ı���ʽ�� ��
��2����ҵ����һ����̼��ȡ�����ķ�ӦΪ��CO(g)+H2O(g) ![]() CO2(g)+H2(g)����֪420��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=9�������Ӧ��ʼʱ����2L���ܱ������г���CO��H2O�����ʵ�������0.60mol��5minĩ�ﵽƽ�⣬���ʱCO��ת����Ϊ ��H2��ƽ����������Ϊ mol��L-1��min-1��
CO2(g)+H2(g)����֪420��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=9�������Ӧ��ʼʱ����2L���ܱ������г���CO��H2O�����ʵ�������0.60mol��5minĩ�ﵽƽ�⣬���ʱCO��ת����Ϊ ��H2��ƽ����������Ϊ mol��L-1��min-1��
��3��Ϊ�������������ʹ������к����庬�����о�������β����CO��NO��CxHy���ŷ��������ش�����β����Ⱦ��ĺ������/ȼ��(������ȼ�����������)�ı仯��ϵ��ͼ��ʾ��

��֪��N2��O2����NO�ķ�Ӧ�����ȷ�Ӧ������ͣ�
�����/ȼ������CO��CxHy�ĺ������ٵ�ԭ���� ��
������/ȼ�ȴﵽ15��NO���ٵ�ԭ������� ��
��4��һ��������H2��CO�ϳ�CH3OH��CH3OH��ת����ΪCH3OCH3��ת�����Ȼ�ѧ��Ӧ����ʽ���£�2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ��H=-24.5 kJ��mol-1
CH3OCH3(g)+H2O(g) ��H=-24.5 kJ��mol-1
��250����ѹǿ������ܱ������У�����2mol��CH3OH��һ��ʱ���������Ӧ��ƽ�⣬��ϵ�ų�����11 kJ����ͬһ�����¼���0.2mol CH3OCH3��0.2mol H2O��һ��ʱ���������Ӧ��ƽ�⣬��ϵ����ЧӦΪ .
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�����ͬλ�ص��ǣ�����ţ���ͬ�� ������ͬ����������� ����Ϊͬϵ����� ������ͬ���칹����� ������ͬ�����ʵ��� ��
A��O2��O3 B.D��T C.![]()
D.![]() E.
E.

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧһѡ��5���л���ѧ����]
�������������һ�־���ҩ��������ʧ��ҩ�����ɷ�����AΪ��ʼԭ�Ϻϳɣ�

![]()
�ش��������⣺
��1��B�Ĺ���������Ϊ____________��D�ķ���ʽΪ____________��
��2����Ӧ�ٵĻ�ѧ����ʽΪ_______________________����Ӧ����Ϊ____________�����������У���Ӧ���������ͬ�Ļ���____________���Ӧ��ţ���
��3����Ӧ�ܳ�������E�⣬��һ�ֲ���Ļ�ѧʽΪ____________��
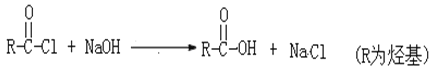
��4��д��ClCH2COCl ��������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ_______________________��
��֪��
��5��C�ķ�����ͬ���칹���У�������ֻ��һ��ȡ�������칹�干��________�֣������������칹�������к˴Ź����������ĸ��壬�ҷ������Ϊ6:2:2:1����______��д�ṹ��ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����̬ͭԭ�ӵĺ���δ�ɶԵ�����ĿΪ___________��
��2�����ݵ�2����Ԫ�ص�һ�����ܵı仯���ɣ�������ͼB��FԪ�ص�λ�ã���С�ڵ���C��N��O����Ԫ�ص����λ�á�

��3��NF3����NH3��F2��Cu���������·�Ӧֱ�ӵõ���
2NH3+3F2![]() NF3+3NH4F
NF3+3NH4F
������ѧ����ʽ�е�5�����������ľ���������___________��
��4��BF3��һ����ˮ�γɣ�H2O��2BF3����Q��Q��һ�������¿�ת��ΪR:
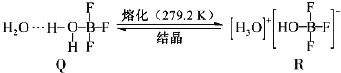
������Q�и��������ǿ�����������___________������ţ���
a�����Ӽ� b�����ۼ� c����λ�� d�������� e����� f�����»���
��R�������ӵĿռ乹��Ϊ___________�������ӵ�����ԭ�ӹ������1��2sԭ�ӹ����___________��___________ԭ�ӹ���ӻ���
��5����ͭ�ۼ���Ũ��ˮ��.��ͨ����������ַ�Ӧ����Һ�����ɫ��һ��ͭ���ӵ���λ�����.
�÷�Ӧ�����ӷ���ʽΪ___________��
��6��������Ϊ�������������ṹ�����ͣ�.�����е���λ��Ϊ___________����������ܶ�Ϊ��g/cm3����ԭ�Ӱ뾶Ϊ___________cm���ú�����NA�Ĵ���ʽ��ʾ�����ػ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com