

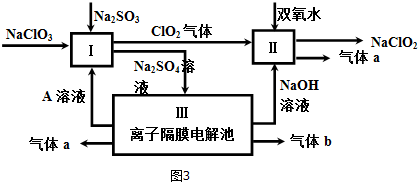
���� ��1��Bװ�������ռ�ClO2����ClO2�۵�ͣ�Ӧ����ˮ��ȴ�ռ���
��2��NaClO2�ܽ�����¶�Ӱ������¶ȸ���38��ʱ����������NaClO2������Һ�л��NaClO2���壬��Ҫ�����ᾧ�����Ȼ�38�����Ϲ��ˡ�ϴ�ӡ�����õ���
��3����������ͼ��֪���������Ӹ�Ĥ���أ������������Һ�����ǵ��ˮ������a����ҺA��ͬһ�缫�õ���NaOH������b������缫�õ�����AΪ���ᣬaΪ������bΪ������I��NaClO3��Na2SO3�����ᷴӦ����C1O2��Na2SO4��Һ����Ӧ���ӷ���ʽΪ��2H++SO32-+2ClO3-=2C1O2+SO42-+H2O������C1O2����������ڼ��������·�Ӧ����NaClO2��������
��ClO2�����������ƺ�ϡ����Ϊԭ���Ʊ������ݵ���ת���غ㣬��֪����NaCl���ɣ�
�۷�����Ӧ��3NaClO2=2NaClO3+NaCl��3molNaClO2���ʵõ�2mol NaClO3��������FeSO4��Һ��Ӧʱ��NaClO2��NaClO3����Fe2+��ԭΪCl-������3molNaClO2��2mol NaClO3��Ӧ��õ�����Ŀ��
��� �⣺��1��Bװ���ռ�ClO2�����۵�ͣ�Ӧ����ˮ��ȴ�ռ���ʹClO2������������ٻӷ���
�ʴ�Ϊ��ʹClO2������������ٻӷ���
��2��NaClO2�ܽ�����¶�Ӱ������¶ȸ���38��ʱ����������NaClO2������Һ�л��NaClO2���壬��Ҫ�����ᾧ�����Ȼ�38�����Ϲ��ˡ�ϴ�ӡ�����õ���
�ʴ�Ϊ�������ᾧ�����ȹ��ˣ�
��3����������ͼ��֪���������Ӹ�Ĥ���أ������������Һ�����ǵ��ˮ������a����ҺA��ͬһ�缫�õ���NaOH������b������缫�õ�����AΪ���ᣬaΪ������bΪ������I��NaClO3��Na2SO3�����ᷴӦ����C1O2��Na2SO4��Һ����Ӧ���ӷ���ʽΪ��2H++SO32-+2ClO3-=2C1O2+SO42-+H2O������C1O2����������ڼ��������·�Ӧ����NaClO2�����������з�Ӧ���ӷ���ʽΪ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O��
�ʴ�Ϊ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O��
��ClO2�����������ƺ�ϡ����Ϊԭ���Ʊ������ݵ���ת���غ㣬��֪����NaCl���ɣ���Ӧ����ʽΪ��5NaClO2+4HCl=5NaCl+4ClO2��+2H2O��
�ʴ�Ϊ��5NaClO2+4HCl=5NaCl+4ClO2��+2H2O��
�۷�����Ӧ��3NaClO2=2NaClO3+NaCl��3molNaClO2���ʵõ�2mol NaClO3��������FeSO4��Һ��Ӧʱ��NaClO2��NaClO3����Fe2+��ԭΪCl-��3molNaClO2��Ӧ��õ���Ϊ3mol��4=12mol��2mol NaClO3��Ӧ��õ���Ϊ2mol��6-12mol��������Fe2+���ʵ�����ͬ��
�ʴ�Ϊ����ͬ��
���� ���⿼�������Ʊ�ʵ�鷽������ƣ���Ŀ�Ѷ��еȣ����ض��Ʊ�ԭ�������ʵķ����ᴿ�Ŀ��飬�ϺõĿ���ѧ���������⡢����������������ȷʵ��Ŀ�ġ�ʵ��ԭ��Ϊ���ؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 24 | B�� | 25 | C�� | 26 | D�� | 27 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
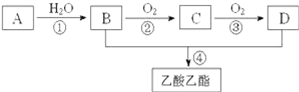
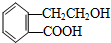 ������ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D��E�������ʣ�
������ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D��E�������ʣ�
 ��
��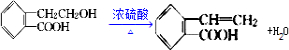 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���³�ѹ�£�11.2L�����������е�ԭ����ΪNA | |
| B�� | 17g��NH3�����к��еĵ�����Ϊ10NA | |
| C�� | ���³�ѹ�£�48g O3���е���ԭ����Ϊ3NA | |
| D�� | ��״���£�11.2LH2O�������еķ�����Ϊ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4��-CH3��������4��һ��ȡ���� | B�� | 3��-CH3��������3��һ��ȡ���� | ||
| C�� | 3��-CH3��������4��һ��ȡ���� | D�� | 2��-CH3��������4��һ��ȡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ģ���������ý������������� | |
| B�� | ���������������HCO3-������������� | |
| C�� | ��Ϊͭ���������ã�����ͭ���Ȼ�����Һ���ᷢ����ѧ��Ӧ | |
| D�� | úȼ��ǰ����������ʯ�ҿ��Լ�����Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ����10.00 mL | B�� | С��10.00 mL | C�� | ����10.00 mL | D�� | ����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com