


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:不详 题型:单选题

| A.电池工作时,H+向电池的负极迁移 |
| B.电池工作时,电流由a极沿导线流向b极 |
| C.a极上发生的电极反应是:C2H5OH+3H2O+12e-=2CO2+12H+ |
| D.b极上发生的电极反应是:4H++O2+4e-=2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.正极反应为:Zn—2e-=Zn2+ |
| B.电池反应为:Zn+Cu2+=Zn2+ +Cu |
| C.在外电路中,电子从正极流向负极 |
| D.盐桥中的K+移向ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
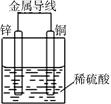
| A.氢离子在负极得电子 |
| B.锌为负极,发生氧化反应 |
| C.铜为负极,铜片上有气泡产生 |
| D.电子从铜极流向锌极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
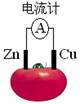
| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.番茄中的阴离子移向铜 | D.锌电极是该电池的正极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.充电电池充电时,发生电解池反应;放电时,发生原电池反应 |
| B.电镀时,应将镀层金属与电源正极相连 |
| C.电解饱和NaCl溶液时,阳极上放出黄绿色气体的同时还产生大量的氢氧化钠 |
| D.利用电化学原理保护金属主要有两种方法,分别是牺牲阳极的阴极保护法和外加电流的阴极保护法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com