
欲配制pH=10.00的NH3和NH4Cl缓冲溶液1升,已知用去1.5mol?L-1NH3?H2O 350 mL, 则需要NH4Cl多少克? 已知: NH3的Kb=1.8×10-5, NH4Cl的式量为 53.5.
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 滴定次数 实验数据 |
1 | 2 | 3 | 4 |
| V(醋酸溶液)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.00 | 0.200 | 0.10 | 0.00 |
| V(NaOH)/mL(终读数) | 14.98 | 15.20 | 15.12 | 15.95 |

查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省涟水中学高二5月学分认定模块检测化学试卷(带解析) 题型:填空题
已知金属离子从开始形成氢氧化物沉淀到沉淀完全时溶液的pH。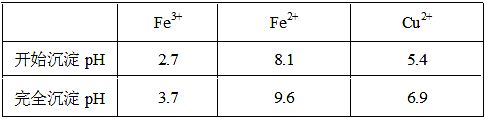
(1)实验室配制FeCl2溶液时需加入少许盐酸和铁粉,若只加盐酸、不加铁粉,溶液中会发生什么变化,用离子方程式表示为: ;
(2)氯化铜晶体(CuCl2·2H2O)中含FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下面所示的操作步骤进行提纯。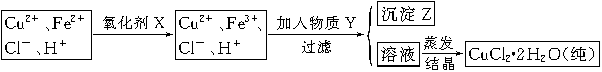
①加氧化剂X的目的是 ,下列氧化剂中最适合作氧化剂X的是 (填序号);
| A.NaClO | B.H2O2 | C.KMnO4 | D.HNO3 |
查看答案和解析>>
科目:高中化学 来源:2014届江苏省高二5月学分认定模块检测化学试卷(解析版) 题型:填空题
已知金属离子从开始形成氢氧化物沉淀到沉淀完全时溶液的pH。

(1)实验室配制FeCl2溶液时需加入少许盐酸和铁粉,若只加盐酸、不加铁粉,溶液中会发生什么变化,用离子方程式表示为: ;
(2)氯化铜晶体(CuCl2·2H2O)中含FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下面所示的操作步骤进行提纯。

①加氧化剂X的目的是 ,下列氧化剂中最适合作氧化剂X的是 (填序号);
A.NaClO B.H2O2 C.KMnO4 D.HNO3
②物质Y的化学式是 ;加入物质Y的目的是调节溶液的pH至a,使Fe3+沉淀完全,则a的范围是 ;若25℃时,a=3的溶液中,c(Fe3+)= mol·L-1。(25℃时,Ksp[Fe(OH)3]=4.0×10-38)
(3)欲将CuCl2·2H2O加热制得无水CuCl2,将采用什么方法和措施?__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08温州市八校联考)
(Ⅰ)(4分) 下列有关化学实验的说法正确的是(填序号) 。
A.滴定用的锥形瓶和滴定管都要用所盛溶液润洗
B.制备(收集)任何气体开始实验前,都要首先检查装置的气密性
C.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次
D.测定溶液的pH时,应先将pH试纸润湿
E.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸
F.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
(Ⅱ)(11分)下图甲是旧教材中验证铜与浓硝酸反应的装置,乙是新教材对演示实验改进后的装置,丙是某校师生对乙作进一步改进并对所产生的气体的性质进行探究的装置。

(1)与甲装置相比,乙装置的优点是 , 丙装置除具乙装置优点外还具有的优点是 。(写出一点即可)
(2)欲使NO2气体充满试管②,应先关闭弹簧夹 ,再打开弹簧夹 ,当气体充满②后,将铜丝提起与溶液脱离,然后把a、b、c都关闭,并把试管②置于沸水中,下列情况不变的是 。
A.颜色 B.平均摩尔质量 C.压强 D.密度
(3)为了验证NO2与水的反应,欲使烧杯中的水进入试管②的操作是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
欲配制500 mL pH=9且含[NH4+]为1 mol?L-1的缓冲溶液,需密度是0.904克/厘米,浓度为26.0%的浓氨水(mL)和固体NH4Cl(式量为53.5)分别是多少? 已知: K=1.88×10-5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com