
 .
. 分析 (1)根据价层电子对互斥理论确定N、C原子的杂化方式及CO32-的空间构型,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数;
(2)Ca原子的M能层有8个电子和N能层有2个电子;
(3)比较两种元素的非金属性强弱,可根据单质之间的置换反应、与氢气反应的难易程度、氢化物的稳定性以及最高正价氧化物对应水化物酸性强弱等角度,元素的非金属性越强,则对应的最高价氧化物对应水化物的酸性越强;同一主族元素氢化物中,氢化物的沸点随着原子序数增大而呈增大趋势,但含有氢键的氢化物熔沸点最高;
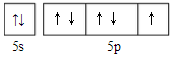
(4)碘是53号元素,其原子核外有53个电子,5S、5P电子为其价电子,根据构造原理书写其价电子排布图.
解答 解:(1)(NH4)2CO3中铵根离子中N原子价层电子对个数是4,不含孤电子对,所以N原子杂化方式是sp3杂化,CO32-中σ键个数=配原子个数=3,孤电子对个数=$\frac{1}{2}$(4+2-3×2)=0,碳原子的价层电子数=3+$\frac{1}{2}$(4+2-3×2)=3,不含孤电子对,所以C采取sp2杂化,轨道构型为平面正三角形,空间构型为平面正三角形;
故答案为:sp3杂化;sp2杂化;平面正三角形;
(2)Ca原子的M能层有8个电子和N能层有2个电子,M层排满应该是18个电子,N层排满应该是32个电子,所以没有排满的电子层为M能层和N能层;
故答案为:M能层和N能层;
(3)N、P位于相同主族,非金属性N>P,元素的非金属性越强,对应的最高高价氧化物的水化物的酸性越强,则酸性HNO3>H3PO4,同一主族元素氢化物中,氢化物的沸点随着原子序数增大而呈增大趋势,但含有氢键的氢化物熔沸点最高,同一周期元素氢化物中,含有氢键的氢化物沸点较高,NH3 分子间易形成氢键,而pH3 分子间不能 形成氢键,所以NH3 沸点更高,
故答案为:HNO3>H3PO4;NH3 ;NH3 分子间易形成氢键;
(4)碘是53号元素,价电子排布为5s25P6,价电子排布图是 ,
,
故答案为: .
.
点评 本题考查了物质结构与性质,涉及杂化方式、离子的空间构型、核外电子排布、等,旨在考查学生对基础知识的掌握,侧重考查分析能力及知识应用能力,题目难度中等.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3是某些胃药的一种成分 | |
| B. | 乳酸铁是某些补铁口服液的有效成分 | |
| C. | 臭氧可以作为新型自来水消毒剂 | |
| D. | SO2常用作红葡萄酒中杀菌消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CO、2mol H2 | 1mol CH3OH | 2mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | 2c1>c3 | B. | a+b=90.7 | C. | 2V2<V3 | D. | α1+α3=0.75 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅酸可使紫色石蕊试液变红色 | |
| B. | 二氧化硫通入紫色石蕊试液中.试液先变红后褪色 | |
| C. | 可用锌粒与稀硝酸反应制备氢气 | |
| D. | 液溴易挥发,所以存放液溴的试剂瓶中应加水封保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y |
| Z | W |
| A. | 若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数) | |
| B. | 若四种元素均为非金属,则W的最高价氧化物对应水化物一定为强酸 | |
| C. | 若四种元素中只有一种为金属,则Y的最高价氧化物对应水化物一定为强酸 | |
| D. | 若四种元素均为金属,则Z的最高价氧化物对应水化物一定为强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3是反应的还原剂 | |
| B. | Na2O2既是氧化剂又是还原剂 | |
| C. | Na2FeO4是反应的氧化产物 | |
| D. | 氧化剂与还原剂的物质的量的比是3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ③⑤ | D. | ②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com