
| A、铝合金 | B、高温结构氮化硅陶瓷 |
| C、有机玻璃 | D、砖瓦 |
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
| A、向溶液中加滴加几滴浓盐酸,c(NH4+)减少 |
| B、向溶液中加入少量CH3COONa固体,c(NH4+)减少 |
| C、溶液中离子浓度关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、向溶液中加适量氨水使混合液的pH=7,混合液中c(NH4+)>c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 符号 | 元素原子结构 |
X | 原子结构示意图为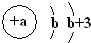 |
| Y | 最外层电子数是次外层电子数的2倍 |
Z | 原子核内含有12个中子,且其离子的结构示意图为  |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、乙醇分子中甲基的电子式为 |
| B、乙醇结构简式为:C2H6O |
C、乙醇分子中羟基电子式: |
D、乙醇分子的比例模型为: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、适量Na2O2与CO2反应,生成1molO2时,转移的电子数为2NA |
| B、1mol甲醇中含有的C-H的数目为4NA |
| C、25℃时,pH=2的硫酸溶液中,含有的H+的数目为0.01NA |
| D、某密闭容器中有2molSO2和1molO2,在一定条件下充分反应,转移的电子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 浓硫酸 |
| △ |
| 加热方式 | 通CO加热 时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
| 样品序号 | 加热方式 | 元素组成和质量分数 |
| 产物样品I | 酒精灯 | w(Fe)=74.4%、w(O)=25.6% |
| 产物样品II | 酒精喷灯 | w(Fe)=100% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 立方烷是一种新合成的烃,其分子为正立方体结构,其碳架结构如图所示
立方烷是一种新合成的烃,其分子为正立方体结构,其碳架结构如图所示查看答案和解析>>
科目:高中化学 来源: 题型:
 按要求回答下列问题:
按要求回答下列问题:+ 4 |
| c(CH3COO-) |
| c(CH3COOH)?c(OH-) |
| c(CH3COO-) |
| c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com