
| A. | $\frac{1}{22.4}$mol/L | B. | $\frac{1}{44.8}$mol/L | C. | $\frac{1}{33.6}$mol/L | D. | 无法计算 |
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | “类钫”在化合物中呈+1价 | |
| B. | 类钫具有放射性 | |
| C. | 单质与水反应较为缓慢 | |
| D. | 类钫最高价氧化物对应的水化物是强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
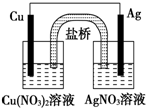
| A. | 将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同 | |
| B. | 该电池的负极反应为:Ag++e-═Ag | |
| C. | 在外电路中,电子由银电极流向铜电极 | |
| D. | 实验过程中取出盐桥,原电池仍继续工作 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3 和Al3+ | B. | Al(OH)3 和AlO2- | C. | 全部为Al(OH)3 | D. | 全部为AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-、NH4+、H+、Cl- | B. | AlO2-、OH-、Na+、Cl- | ||
| C. | AlO2-、H+、MnO4-、NO3- | D. | Mg2+、Fe3+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可使溴水溶液褪色 | B. | 不能与酸性高锰酸钾溶液反应 | ||
| C. | 能发生银镜反应 | D. | 一定条件下能发生加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
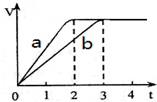 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图所示,下列说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图所示,下列说法正确的是( )| A. | 曲线a代表Al的反应过程,曲线b代表Mg的反应过程 | |
| B. | Mg和Al的质量之比为3:2 | |
| C. | Mg和Al的物质的量之比为3:2 | |
| D. | Mg和Al的反应速率之比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com