
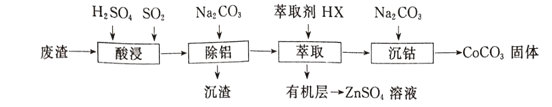
【题目】CoCO3可用作选矿剂、催化剂及家装涂料的颜料。以含钴废渣(主要成CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
下表是相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol/L计算):
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Co2+ | 7.6 | 9.4 |
Al3+ | 3.0 | 5.0 |
Zn2+ | 5.4 | 8.0 |
(1)写出“酸溶”时发生氧化还原反应的化学方程式____________________。
(2)“除铝”过程中需要调节溶液pH的范围为_______________ 。
(3)在实验室里,萃取操作用到的玻璃仪器主要有____;上述“萃取”过程可表示为ZnSO4(水层)+2HX(有机层) ![]() ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是______。
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是______。
(4)简述洗涤沉淀的操作____________________________________。
(5)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为 ____________________。
【答案】Co2O3+SO2+H2SO4=2CoSO4+H2O 5.0~5.4 分液漏斗、烧杯 向有机层中加入适量的硫酸溶液充分振荡,静置,分离出水层 向漏斗中加蒸馏水至没过沉淀,待水自然流完后,重复上述操作2-3次 Co3O4
【解析】
(1)从最终产物看,酸溶时,Co2O3被还原为Co2+,SO2被氧化为SO42-,
“酸溶”时发生氧化还原反应的化学方程式Co2O3+SO2+H2SO4=2CoSO4+H2O。
答案为:Co2O3+SO2+H2SO4=2CoSO4+H2O
(2)“除铝”过程中需要调节溶液pH的范围,目的是让Al3+全部转化为沉淀,而Zn2+不生成沉淀,所以pH的范围应为5.0~5.4。答案为:5.0~5.4
(3)在实验室里,萃取操作用到的玻璃仪器主要有分液漏斗、烧杯。
答案为:分液漏斗、烧杯
上述“萃取”过程可表示为ZnSO4(水层)+2HX(有机层) ![]() ZnX2(有机层)+H2SO4(水层),从反应中可以看出,此反应为可逆反应,所以加硫酸可实现让ZnSO4进入水层的目的。从而得出由有机层获取ZnSO4溶液的操作是向有机层中加入适量的硫酸溶液充分振荡,静置,分离出水层。
ZnX2(有机层)+H2SO4(水层),从反应中可以看出,此反应为可逆反应,所以加硫酸可实现让ZnSO4进入水层的目的。从而得出由有机层获取ZnSO4溶液的操作是向有机层中加入适量的硫酸溶液充分振荡,静置,分离出水层。
答案为:向有机层中加入适量的硫酸溶液充分振荡,静置,分离出水层
(4)洗涤沉淀的操作是:向漏斗中加蒸馏水至没过沉淀,待水自然流完后,重复上述操作2-3次。
答案为:向漏斗中加蒸馏水至没过沉淀,待水自然流完后,重复上述操作2-3次。
(5)从化学式CoCO3可以看出,n(Co)=n(C)=![]() ,
,
m(Co)=0.03mol×59g/mol=1.77g
m(O)=2.41g-1.77g=0.64g
n(O)=![]()
n(Co):n(O)= 0.03mol:0.04mol=3:4
则该钴氧化物的化学式为Co3O4。
答案为:Co3O4


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,则下列叙述中正确的是( )
A.同温同压下,NA个NO气体与NA个N2和O2的混合气体的体积相等
B.标准状况下,22.4LCCl4所含分子数为NA
C.4℃时,9mL水和标准状况下11.2L氮气含有相同的原子数
D.1.7gH2O2中含有的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是( )
A.可用水来确定某氧化钠粉末中是否含有过氧化钠
B.可用二氧化碳来确定某氧化钠粉末中是否含有过氧化钠
C.可利用在空气中加热的方法除去氧化钠中的过氧化钠
D.将足量的过氧化钠、氧化钠分别加到酚酞溶液中,最终溶液均为红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 向![]() 溶液中加入少量氨水:
溶液中加入少量氨水:![]() ==Al(OH)3
==Al(OH)3![]()
B. 向![]() 溶液中加入KOH溶液:HCO3-+OH-═H2O+CO2↑
溶液中加入KOH溶液:HCO3-+OH-═H2O+CO2↑
C. 向![]() 溶液中加入过量的NaOH溶液:
溶液中加入过量的NaOH溶液:![]()
D. 向![]() 溶液中加入过量澄清石灰水:
溶液中加入过量澄清石灰水:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na2S2O3)溶解,反应生成Na3[Ag(S2O3)2];在废定影液中加入Na2S使Na3[Ag(S2O3)2]中的银转化为Ag2S,并使定影液再生。将Ag2S在高温下转化为Ag,就达到了回收银的目的。
(1)铜、银、金在元素周期表中位于同一族相邻周期,基态铜原子的价电子排布式为___。
(2)Na、O、S简单离子半径由大到小的顺序为___。
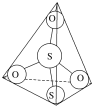
(3)S2O32-离子结构如图所示,其中心硫原子的杂化轨道类型为___。
(4)Na3[Ag(S2O3)2]中存在的作用力有__。
A.离子键 B.共价键 C.范德华力 D.金属键 E.配位键
(5)在空气中灼烧Ag2S生成Ag和SO2,SO2分子中硫原子的价层电子对数为__,其分子空间构型为___。SO2易溶于水,原因是__。
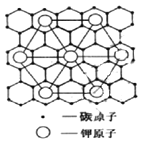
(6)SO2具有较强的还原性,碳与熔融金属钾作用,形成的晶体是已知最强的还原剂之一,碳的某种晶体为层状结构,钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图所示,则其化学式可表示为___。
(7)现在人们已经有多种方法来测定阿伏加德罗常数,X射线衍射法就是其中的一种,通过对金晶体的X 射线衍射图像的分析,可以得出金晶体的晶胞属于面心立方晶胞(与铜的晶胞相似)。若金原子的半径为am,金的密度为ρg·cm-3,金的摩尔质量为Mg·mol-1,试通过这些数据列出计算阿伏加德罗常数的算式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数。
样品12.0 g ![]() 溶液
溶液![]() 沉淀
沉淀![]() 固体19.7 g
固体19.7 g
(1)如何检验氯化钡溶液已过量____________
(2)检验沉淀是否洗涤干净所用到的试剂是____________
(3)样品中Na2CO3的质量分数为_________(小数点后保留1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述,不正确的是
A. 正戊烷、异戊烷、新戊烷的沸点依次降低
B. 相对分子质量为104的烃,分子中不可能只存在单键
C. 光照下2,2一二甲基丙烷与Br2反应其二溴取代物有两种
D. FeCl3溶液可以把4种无色溶液:乙醇、苯酚、AgNO3溶液、KOH溶液一一区分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 、
、![]() 、
、![]() 为原子序数依次增大的短周期元素,
为原子序数依次增大的短周期元素,![]() 为地壳中含量最高的过渡金属元素,
为地壳中含量最高的过渡金属元素,![]() 与
与![]() 同主族,
同主族,![]() 与
与![]() 同周期,且
同周期,且![]() 与
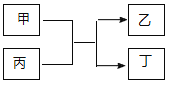
与![]() 的原子序数之和为20。甲、乙分别为元素E、A的单质, 丙、丁为A、E分别与B形成的二元化合物,它们转化关系如图所示。下列说法不正确的是( )
的原子序数之和为20。甲、乙分别为元素E、A的单质, 丙、丁为A、E分别与B形成的二元化合物,它们转化关系如图所示。下列说法不正确的是( )
A.![]() 、
、![]() 形成的一种化合物具有漂白性
形成的一种化合物具有漂白性
B.![]() 、
、![]() 形成的离子化合物可能含有非极性键
形成的离子化合物可能含有非极性键
C.![]() 的单质能与丙反应置换出
的单质能与丙反应置换出![]() 的单质
的单质
D.丁为黑色固体,且1mol甲与足量丙反应转移电子3 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com