
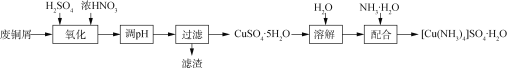
【题目】实验室以废铜屑(含少量Fe、不溶性杂质)为原料制取CuSO4·5H2O晶体和[Cu(NH3)4]SO4·H2O晶体,其实验流程如下:
(1)氧化时先加入一定量3 mol/L H2SO4,再调节浓硝酸的用量至![]() 为2.0左右时,铜粉和浓硝酸完全反应,主要反应的化学方程式为_______。
为2.0左右时,铜粉和浓硝酸完全反应,主要反应的化学方程式为_______。
硝酸过量对产品的影响为________________________________。
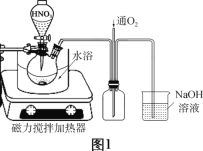
(2)废铜屑的氧化在如图1所示的装置中进行。从长导管中通入氧气的作用是___________。保持试剂的用量不变,实验中提高Cu转化率的操作有____________(写一种)。
(3)调节溶液pH应在3.5~4.5范围的原因是______________________。
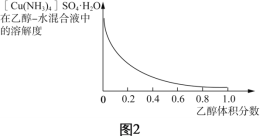
(4)已知:[Cu(NH3)4]2+![]() Cu2++4NH3;CuSO4、(NH4)2SO4难溶于乙醇。结合图2,[Cu(NH3)4]SO4·H2O在乙醇水混合液中的溶解度随乙醇浓度变化曲线,补充完整由加足量氨水后所得的[Cu(NH3)4]SO4溶液制备[Cu(NH3)4]SO4·H2O晶体的实验方案:______________ (实验中必须使用的试剂和仪器:无水乙醇、乙醇-水混合液、BaCl2溶液、真空干燥箱)。
Cu2++4NH3;CuSO4、(NH4)2SO4难溶于乙醇。结合图2,[Cu(NH3)4]SO4·H2O在乙醇水混合液中的溶解度随乙醇浓度变化曲线,补充完整由加足量氨水后所得的[Cu(NH3)4]SO4溶液制备[Cu(NH3)4]SO4·H2O晶体的实验方案:______________ (实验中必须使用的试剂和仪器:无水乙醇、乙醇-水混合液、BaCl2溶液、真空干燥箱)。
【答案】Cu+2HNO3+H2SO4![]() CuSO4+2NO2↑+2H2O 降低产品的产率和纯度 防止倒吸,使尾气中的氮氧化物能被完全吸收 适当提高反应温度、加快搅拌速率 使Fe3+完全水解转化为Fe(OH)3沉淀除去,而Cu2+留在溶液中 将[Cu(NH3)4]SO4溶液加入无水乙醇中,过滤,所得沉淀先用乙醇-水混合液洗涤,至最后的洗涤滤液中滴加BaCl2溶液无沉淀生成,再将晶体用无水乙醇洗涤,放入真空干燥箱中干燥
CuSO4+2NO2↑+2H2O 降低产品的产率和纯度 防止倒吸,使尾气中的氮氧化物能被完全吸收 适当提高反应温度、加快搅拌速率 使Fe3+完全水解转化为Fe(OH)3沉淀除去,而Cu2+留在溶液中 将[Cu(NH3)4]SO4溶液加入无水乙醇中,过滤,所得沉淀先用乙醇-水混合液洗涤,至最后的洗涤滤液中滴加BaCl2溶液无沉淀生成,再将晶体用无水乙醇洗涤,放入真空干燥箱中干燥
【解析】
(1)Cu与浓硝酸、硫酸发生氧化还原反应产生CuSO4、NO2和H2O,根据原子守恒、电子守恒书写反应方程式;结合物质成分分析Cu、HNO3的物质的量比例关系;
(2)从安全角度和环保角度分析通入O2的原因;根据影响反应速率的因素分析;
(3)根据Fe3+、Cu2+形成沉淀需要的溶液的pH分析;
(4)根据CuSO4、(NH4)2SO4、[Cu(NH3)4]SO4·H2O难溶于乙醇,乙溶于水,而[Cu(NH3)4]SO4·H2O在乙醇与水混合溶液中的溶解度随乙醇含量的增大而减小分析。
(1) Cu与浓硝酸、硫酸发生氧化还原反应产生CuSO4、NO2和H2O,根据原子守恒、电子守恒书写反应方程式为Cu+2HNO3+H2SO4![]() CuSO4+2NO2↑+2H2O;在反应时为保证制取的CuSO4纯度,要严格控制HNO3的用量,尽可能使硝酸完全反应转化为NO2气体逸出,若硝酸过量,则反应后的溶液中含有过量的硝酸,则制取得到的CuSO4产品中混有Cu(NO3)2,导致产品的纯度降低,且会是CuSO4的产率也减小;
CuSO4+2NO2↑+2H2O;在反应时为保证制取的CuSO4纯度,要严格控制HNO3的用量,尽可能使硝酸完全反应转化为NO2气体逸出,若硝酸过量,则反应后的溶液中含有过量的硝酸,则制取得到的CuSO4产品中混有Cu(NO3)2,导致产品的纯度降低,且会是CuSO4的产率也减小;
(2)从长导管中通入氧气,可以防止因NO2在NaOH溶液中的溶解而产生的装置内气体压强减小,从而引起倒吸现象的发生;且能使反应产生的NO反应变为NO2,再被NaOH溶液完全吸收,就避免了氮氧化合物对大气造成的污染;
Cu是固体物质,在保持试剂的用量不变,在实验中若要提高Cu转化率,可通过适当提高反应温度、加快搅拌速率使反应物充分接触实现;
(3)在废铜屑中含少量Fe,在用浓硝酸与硫酸混合液氧化Cu时,Fe被氧化变为Fe3+,由于Fe3+形成Fe(OH)3沉淀,沉淀完全时溶液的pH=3.2,调节溶液pH应在3.5~4.5范围,就可以使Fe3+完全转化为Fe(OH)3沉淀除去,而Cu2+仍留在溶液中,以保证制取得到纯净的CuSO4;
(4)将制得的[Cu(NH3)4]SO4溶液加入无水乙醇中,由图象可知[Cu(NH3)4]SO4·H2O在无水乙醇中不能溶解,就会析出[Cu(NH3)4]SO4·H2O沉淀,然后过滤得到[Cu(NH3)4]SO4·H2O沉淀,所得沉淀中混有杂质CuSO4、(NH4)2SO4,先用乙醇-水混合液洗涤,除去杂质,然后根据BaSO4是白色不溶于水的沉淀,通过检验洗涤液中是否含有SO42-,来判断沉淀是否洗涤干净,向最后的洗涤滤液中滴加BaCl2溶液无沉淀生成,说明沉淀洗涤干净,最后再将晶体用无水乙醇洗涤,放入真空干燥箱中干燥,就得到[Cu(NH3)4]SO4·H2O。


科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
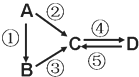
(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出②反应的离子方程式_________;④反应离子方程式__________。
(2)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水高温下反应的化学方程式_______________________。④反应的离子方程式______________。D中加入氢氧化钠的现象__________。
(3)若A是太阳能电池用的光伏材料,B常用用于制作高档光学器材,C、D为钠盐,C的水溶液俗称泡花碱,D的溶液显碱性。④反应也是通入一种引起温室效应的主要气体。写出③反应的化学方程式________________________。⑤反应用到B,反应条件为高温,则⑤的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25 mL 2 mol·L-1Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中 ②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况( )
A.均为0.84 L
B.均为0.56 L
C.①>②
D.②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1906年,哈伯在60℃高温、200兆帕高压的条件下,用锇(Os)作催化剂,首次成功得到了氨,但产率较低。随着科学的进步以及科学家们对催化剂的研究改进,现在工业上普遍采用铁触媒(主要成分为Fe3O4,助催化剂:K2O、Al2O3、CaO、MgO、CoO等)做合成氨的催化剂,大大提高了合成氨的产率。回答下列问题:
(1)已知元素Co(钴)的原子核内有27个质子,则该元素基态原子价电子排布式为___。
(2)元素Fe的基态原子核外未成对电子数为___;Fe2+与Fe3+相比较,___更稳定。
(3)C、N、O处于同一周期,其中第一电离能最大的___,电负性最大的是___,它们与氢形成的简单氢化物沸点从高到低的顺序为___。
(4)NH3分子中N原子的杂化方式为___;氨气极易溶于水(溶解度1:700),除了氨气能与水发生反应外,还有两个原因分别是___、___。
(5)我国长征系列运载火箭使用的液态燃料主要是偏二甲肼[结构简式:(CH3)2NNH2,可看作是肼(NH2NH2)中同一氮原子上的两个氢原子被甲基取代]和四氧化二氮,燃烧时发生反应:(CH3)2NNH2+2N2O4=2CO2+4H2O+3N2。当该反应消耗1molN2O4时将形成___molπ键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜铁及其化合物在日常生活和工业生产中有着重要用途。
(1)铁制炊具在潮湿的空气中易发生吸氧腐蚀而生锈,负极的电极反应式为:___,正极的电极反应式为:___。
(2)下列哪些装置可防止铁棒被腐蚀___。(填正确答案标号)
A.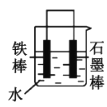 B.
B.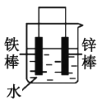 C.
C.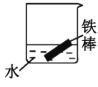 D.
D.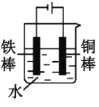
(3)高铁酸钾(K2FeO4)广泛应用于净水、电池工业等领域。工业上以钛白粉生产的副产品FeSO4制备高铁酸钾的生产流程如图:
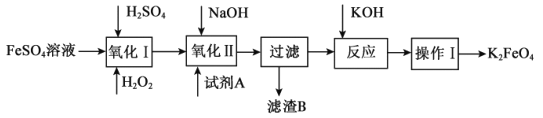
查阅资料:K2FeO4在水中溶解度很大,在碱性环境中稳定,在中性和酸性条件下不稳定。
①“氧化I”中,生成Fe3+的离子反应方程式是___。
②净水时高铁酸钾能逐渐与水反应生成絮状的Fe(OH)3,请补充并配平该反应方程式: K2FeO4+ H2O= Fe(OH)3↓+ KOH+ 。___。
(4)工业上常以铜做阳极,石墨做阴极,电解含有NaOH的NaCl水溶液制备Cu2O。
已知:该电解过程中阳极先生成难溶物CuCl,再与NaOH反应转化为Cu2O。
①写出阳极的电极反应式___,该过程中生成Cu2O的离子反应方程式为___。
②如果电解后溶液体积未发生变化,电解后溶液中的c(OH-)会___(填“变大”“变小”或“不变”)。
③若电解时电路中通过0.2mol电子,理论上生成Cu2O的质量为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是

A. 断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl—![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl—
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Y是一种药物中间体,可由X制得:
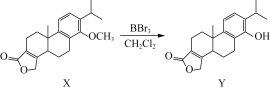
下列有关化合物X、Y的说法正确的是( )
A.Y分子中五元环上的4个碳原子一定共平面
B.1 mol X最多能与2 mol Br2反应
C.用FeCl3溶液可鉴别化合物X和Y
D.X、Y在酸性条件下的水解产物均能发生氧化反应、加成反应、消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业上使用的印刷电路板,是在敷有铜膜的塑料板上以涂层保护所要的线路,然后用三氯化铁浓溶液作用掉(腐蚀)未受保护的铜膜后形成的。某工程师为了从使用过的腐蚀废液(含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费)中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用,准备采用下列步骤:
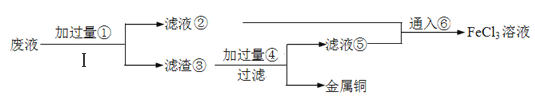
(1)步骤Ⅰ的操作名称:________;所需玻璃仪器:_________、_________、__________。
(2)写出FeCl3溶液与铜箔发生反应的离子方程式:______________________。
(3)检验废腐蚀液中是否含有Fe3+所需试剂名称:___________、实验现象:__________。
(4)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:________________,此转化的化学方程式为:______________________________。
(5)写出③中所含物质:_________⑥发生反应的离子方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把 NaOH、MgCl2、AlCl3 三种固体组成的混合物溶于足量水后,产生 1.16g 白色沉淀, 再向所得浊液中逐渐加入 2.00mol/LHCl 溶液,加入HCl 溶液的体积与生成沉淀的关系如图所示。
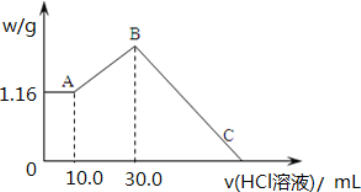
(1)A 点沉淀物的化学式为_____。B 点纵坐标为___________________。
(2)A 点至B 点改为通入二氧化碳气体,至少须标准状况下二氧化碳_____mL。此时发生反应的离子方程式为_____。
(3)B 点含溶质的物质的量是_____mol。C 点(此时沉淀恰好完全溶解)HCl 溶液的体积为_____mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com