
【题目】25℃时,向0.10mol·L-1的H2C2O4(二元弱酸)溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法不正确的是

A. 25℃时H2C2O4的一级电离常数为Ka1=104.3
B. pH=2.7的溶液中:c(H2C2O4)=c(C2O42-)
C. pH=7的溶液中:c(Na+)>2c(C2O42-)
D. 滴加NaOH溶液的过程中始终存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+)
【答案】A
【解析】
草酸属于二元弱酸,滴加NaOH溶液,发生H2C2O4+NaOH=NaHC2O4+H2O,NaHC2O4+NaOH=Na2C2O4+H2O,然后进行分析;
草酸属于二元弱酸,滴加NaOH溶液,发生H2C2O4+NaOH=NaHC2O4+H2O,NaHC2O4+NaOH=Na2C2O4+H2O,
A、根据图像,H2C2O4二级电离常数表达式K=c(C2O42-)×c(H+)/c(HC2O4-),在pH=4.3时,c(C2O42-)=c(HC2O4-),此时H2C2O4的二级电离常数为10-4.3,不是H2C2O4的一级电离常数,故A说法错误;
B、根据图像,pH=2.7的溶液中,c(H2C2O4)=c(C2O42-),故B说法正确;
C、根据电荷守恒,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),当pH=7时,c(H+)=c(OH-),有c(Na+)=c(HC2O4-)+2c(C2O42-),因此c(Na+)>2c(C2O42-),故C说法正确;
D、溶液为电中性,滴加氢氧化钠溶液过程中始终存在c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),故D说法正确;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某盐酸溶液的密度为1.19g/cm3 ,质量分数为36.5%,则该溶液的物质的量浓度为___________
(2)含0.3 mol SO42-的Al2(SO4)3中所含的Al3+的数目为________________。
(3)相同质量的SO2、SO3硫原子的个数之比为_______________ 。
(4)33.3g某二价金属氯化物(ACl2)中含有0.6mol Cl,则ACl2的化学式是_________ 。
(5)标准状况下,1.204×1023个H2的体积约为_______________L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现需要1 mol·L1NaOH溶液240 mL,实验室提供以下试剂用于溶液的配制:蒸馏水、NaOH固体、4mol·L1 NaOH溶液
(1)无论采用何种试剂进行配制,除烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是___________,在使用该仪器前必须进行的操作是_________________。
(2)若用NaOH固体进行配制,需用托盘天平称取NaOH的质量为_______ g;如果用4 mol/L的NaOH溶液稀释配制,需用量筒量取________mL 4mol/LNaOH溶液。
(3)配制一定物质的量浓度的NaOH溶液时,造成所配制溶液浓度偏低的原因是(____)
A. 称量时 NaOH已经潮解
B. 定容时俯视容量瓶的刻度线
C. 向容量瓶中转移溶液时,容量瓶事先用蒸馏水洗涤过
D. 摇匀后发现凹液面低于刻度线,滴加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种将CO2和H2O转换为燃料H2、CO及CH4的装置如图所示(电解质溶液为稀H2SO4)。下列关于该装置的叙述错误的是

A. 该装置可将电能转化为化学能
B. 工作时,电极a周围溶液的pH增大
C. 电极b上生成CH4的电极反应式为CO2+8H++8e-===CH4+2H2O
D. 若电极b上只产生1 mol CO,则通过质子膜的H+数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是( )
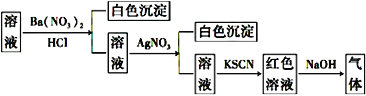
A. 原溶液中一定含有SO42-B. 原溶液中一定含有NH4+
C. 原溶液中一定含有Cl-D. 原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED灯是一种环保的光源,在相同照明效果下比传统光源节能80%以上。目前市售LED晶片材质基本以砷化镓、磷化铝镓钢(AlGaInP)、氮化铟镓( InGaN)为主,砷化镓的晶胞结构如图。回答下列问题:

(1)砷的基态原子的电子排布式是___________。
(2)磷和砷是同一族的元素,第一电离能:磷___________(填“>”“<”或“=”,下同)砷,它们形成的氢化物的沸点:PH3___________AsH3,原因是______________________。
(3)AsH3是无色、稍有大蒜味的气体。AsH3中砷原子的杂化轨道方式为___________,AsH3的空间结构为___________。
(4)砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是_________________________________。
(5)此晶胞中所含的砷原子的个数为___________,砷化镓的化学式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、X、Y、Z是原子序数依次增大的短周期主族元素,Q原子的最外层电子数是内层电子数的2倍,X、Y、Z在周期表中的位置关系如图所示。下列说法正确的是

A. Q和Z可能形成化合物QZ2
B. Y的最高价氧化物的水化物一定是强酸
C. X、Z和氢三种元素不可能组成离子化合物
D. 最简单气态氢化物的沸点:Q>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com