
W、X、y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为________________________________________________________________ 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为________。将等体积、等浓度的W
的最高价氧化物对应的水化物和Y的氢化物混合,其化学方程式为__________________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_____________________________________________________。
(4)W、X、Y、Z四种元素简单离子的离子半径由小到大的顺序是_______________。
(1)Al(OH)3+OH-=AlO2-+2H2O(2分)
(2)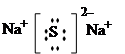 (1分) NaOH+H2S=NaHS+H2O(2分)
(1分) NaOH+H2S=NaHS+H2O(2分)
(3)Cl2+SO2+2H2O=H2SO4+2HCl(2分)
(4)Al3+<Na+< Cl-<S2-(1分)
解析试题分析:(1)W、X是金属元素,且最高价氧化物对应的水化物可以反应生成盐和水,可知W、X分别是Na和Al ,NaOH和Al(OH)3反应生成盐和水。
(2)W与Y可形成化合物W2Y,W是Na,则Y是S, W2Y是Na2S。等物质的量的NaOH和H2S反应生成
NaHS和H2O。
(3) Y的低价氧化物SO2通入Z单质Cl2的水溶液中,发生氧化还原反应,生成H2SO4和HCl。
(4)W、X、Y、Z四种元素分别是Na、Al、S、Cl,所以离子半径由小到大的顺序是Al3+<Na+< Cl-<S2-。
考点:元素周期表和元素周期律。


科目:高中化学 来源: 题型:填空题
自然界中的水要经过消毒杀菌才可成为生活饮用水。ClO2是一种高效安全灭菌消毒剂,
其中Cl化合价为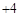 价。
价。
(1)氯原子最外层有 种能量不同的电子,某化合物中O的化合价与ClO2中O的化合价恰好相反,写出该化合物的分子式 。
(2)下列可用作比较S和C非金属性强弱依据的是
A.CS2中各元素的化合价 B.气态氢化物的稳定性
C.元素在周期表中的位置 D.最高价含氧酸的酸性
(3)以下性质的比较正确的是
A.键长:HF>HCl B.稳定性:HF>HCl
C.酸性:HF>HCl D.沸点:HF>HCl
O3也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生反应如下:
反应① O3 O2 +[O]-Q 平衡常数为K1 ;
O2 +[O]-Q 平衡常数为K1 ;
反应② [O]+O3 2O2+Q 平衡常数为K2 ;
2O2+Q 平衡常数为K2 ;
总反应:2O3 3O2+Q 平衡常数为K。
3O2+Q 平衡常数为K。
(4)一定条件下,O3的浓度减少一半所需的时间(t)如下表所示。
已知:O3的起始浓度为0.0216 mol/L。
| pH t / min T / ℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E为五种常见的短周期元素,常温下,A、B可形成B2A2和B2A两种液态化合物,B与D可组成分子X,X水溶液呈碱性,C元素的焰色反应呈黄色,E与C同周期,且E的简单离子半径是同周期元素形成的简单离子中半径最小的。试回答:
(1)D元素在周期表中的位置为 。
(2)B2 A和X的分子结合质子的能力不同,只用一个离子方程式就能证明,写出该离子反应方程式 。
(3)A、D、E三种元素形成的盐(化学式A9D3E)的水溶液呈酸性,用离子方程式解释其原因 ;
(4)W、Q是由A、B、C、D四种元素中任意三种组成的不同类型的强电解质,常温下0.1mol·L—1W的水溶液的pH为13,Q的水溶液呈酸性且能和W反应放出气体,物质的量浓度相同的 W、Q溶液中水的电离程度是前者小于后者。则:W为 ,Q为 (填化学式)。
(5)B和E形成的化合物E2B6常在有机合成中作强还原剂,甚至可将二氧化碳重新还原成甲烷,写出该反应方程式 。
(6)已知工业合成X的反应方程式:D2 (g)+3B2 (g)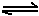 2X(g);△H ="-92.4" kJ·mol-1,在适当的催化剂和恒温恒压条件下反应,下列说法正确的有 。
2X(g);△H ="-92.4" kJ·mol-1,在适当的催化剂和恒温恒压条件下反应,下列说法正确的有 。
A.达到化学平衡时,正逆反应速率相等
B.反应过程中不断分离出X,使平衡常数K减小,平衡正向移动有利于合成X
C.达到平衡后,升高温度,平衡常数K增大,B2的转化率降低
D.达到化学平衡的过程中,气体平均相对分子质量减小
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
四种短周期元素A、B、C、D,原子序数依次增大,结合下列信息:
(1)A的最高价氧化物对应的水化物E与其气态氢化物F反应,得到离子化合物G。
(2)B的焰色应呈黄色。
(3)C在同周期主族元素形成的简单离子中,离子半径最小.
(4)D最高正价与最低负价之和为零.
回答下列问题:
(1)写出D在元素周期表中的位置:
(2)写出化合物F的电子式 ,结构式
(3)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是 (填元素符号)
(4)下列可作为比较元素B和C金属性强弱的依据是 ( 填序号)
a.自然界中的含量b.相应氯化物水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
A的一种氢化物HA3可用于有机合成,其酸性与醋酸相似,体积和浓度均相等的HA3与B的最高价 氧化物对应的水化物的溶液混合,反应的化学方程式是 混合后溶液中离子浓度由大到小的顺序是
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有A、B、C、D、E、五种常见的短周期元素,它们的原子序数依次增大,其中C元素原子最外层电子数是次外层电子数的3倍,B元素原子的最外层电子数比C元素原子的最外层电子数少1个;A和D,C和E同主族,又知C、E两原子序数之和是A、D两原子序数之和的2倍。请回答下列问题:
(1)写出由A、C、D三种元素形成的化合物的电子式 ,该化合物的化学键类型为 。
(2)D2E溶液呈 (填“碱性”、“酸性”、“中性”),试用离子方程式解释原因 。
(3)0.5 L 0.1mol·L—1D的最高价氧化物的水化物与0.25L 0.1 mol·L—1E的最高价氧化物的水化物反应放出2865J的热量,该反应的热化学方程式为: 。
(4)由B的氢化物与C的单质、KOH溶液构成原电池,负极产生B的单质。则其负极电极反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| | W | X | Y | Z |
| 结构或性质 | 最高价氧化物是温室气体,其原子的最外层电子数是次外层电子数的2倍 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 氧化物是常见的两性化合物 | 最高正价与最低负价之和为零 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
短周期主族元素X、Y、Z、W、Q的原子序数依次增大。X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z、W是常见金属,Z的氧化物可做耐火材料,W的简单离子是同周期中离子半径最小的,Q的p能级上有一个未成对电子。试回答下列问题:
(1)比较第一电离能:Z W(填“>”、“<”或“=”,后同);电负性:X Y。
(2)写出Q的价电子排布图 ,YF3的结构式 。
(3)向硫酸铜溶液中逐滴滴入Y的氢化物的水溶液至过量,用离子方程式表示该过程出现的现象变化:
_________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目; W与Y的氧化物均能导致酸雨的形成;Z的非金属性在同周期主族元素中最强。
(1)Y在周期表中的位置是 。
(2)用电子式解释X与W能形成化合物X3W的原因 。
(3)X3W遇水可释放出使酚酞溶液变红的气体A,化学方程式是 。
(4)用惰性电极电解化合物XZ溶液从阴极释放出气体B,反应的离子方程式是 。
(5)已知W的单质与气体B在一定条件下可形成气体A,即: W2 (g)+3B (g)  2A(g) △H =-92.4 kJ?mol―1
2A(g) △H =-92.4 kJ?mol―1
在某温度时,一个容积固定的密闭容器中,发生上述反应。在不同时间测定的容器内各物质的浓度如下表:
| 时间 | 浓度(mol/L) | ||
| c(W2) | c(B) | c(A) | |
| 第0 min | 4.0 | 9.0 | 0 |
| 第10min | 3.8 | 8.4 | 0.4 |
| 第20min | 3.4 | 7.2 | 1.2 |
| 第30min | 3.4 | 7.2 | 1.2 |
| 第40min | 3.6 | 7.8 | 0.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com