
(10分)下列框图中,已知A、E、F、H是单质,其中只有A是固体,其它都是气体,且H是呈黄绿色;B是最常见液体,G的焰色反应呈黄色,L是白色沉淀,M是红褐色沉淀。部分反应的某些产物未标出。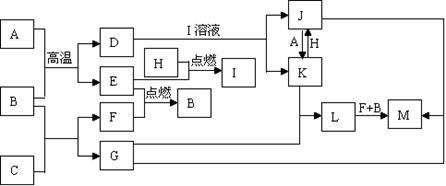
(1)写出H的化学式: 、C的电子式: 。
(2)写出D与I溶液发生反应的离子方程式: 。
(3)写出L→M的化学方程式: 。
(4)检验J中的阳离子时,不宜选用下列试剂中的 (填选项字母)。
A.Fe粉 B.NaOH溶液 C.KSCN溶液
(1)Cl2  (2)Fe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O
(2)Fe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O
(3)4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 (4)A
解析试题分析:根据题意可知A的Fe;B是H2O;D是Fe3O4;E是H2;H是Cl2;I是HCl;C是Na2O2;Na2O2与水反应得到G:NaOH和F:O2;Fe3O4与HCl发生反应得到FeCl2、FeCl3; FeCl2与Cl2发生反应得到FeCl3;FeCl3与Fe发生反应得到FeCl2.因此J是FeCl3;K是FeCl2。NaOH和FeCl2发生反应得到Fe(OH)2和NaCl.根据物质的转化关系可知L是Fe(OH)2;Fe(OH)2与氧气在水存在下发生反应:4Fe(OH)2 + O2+2H2O == 4Fe(OH)3。故M是Fe(OH)3。NaOH与FeCl3也能发生反应得到Fe(OH)3,同时还产生NaCl。(1)H是Cl2;C Na2O2的电子式是 ;(2)根据离子方程式书写的原则,D Fe3O4与HCl溶液发生反应的离子方程式:Fe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O;(3)Fe(OH)2→Fe(OH)3的化学方程式是:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3;(4)检验FeCl3中的阳离子时,A.若加入Fe粉 或Al粉等活泼金属单质时,都会使溶液中的Fe3+变为Fe2+,溶液由黄色变为浅绿色。因此不能选择Fe粉来检验,错误。B.加入NaOH溶液,会发生沉淀反应,产生红褐色Fe(OH)3沉淀。可以鉴别。正确。C.加入KSCN溶液,会发生显色反应:Fe3++3SCN—=Fe(SCN)3,溶液变为血红色。因此可以作鉴别试剂。正确。故选项为A。
;(2)根据离子方程式书写的原则,D Fe3O4与HCl溶液发生反应的离子方程式:Fe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O;(3)Fe(OH)2→Fe(OH)3的化学方程式是:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3;(4)检验FeCl3中的阳离子时,A.若加入Fe粉 或Al粉等活泼金属单质时,都会使溶液中的Fe3+变为Fe2+,溶液由黄色变为浅绿色。因此不能选择Fe粉来检验,错误。B.加入NaOH溶液,会发生沉淀反应,产生红褐色Fe(OH)3沉淀。可以鉴别。正确。C.加入KSCN溶液,会发生显色反应:Fe3++3SCN—=Fe(SCN)3,溶液变为血红色。因此可以作鉴别试剂。正确。故选项为A。
考点:考查元素集化合物的推断、电子式、化学方程式、离子方程式的书写、离子的检验的方法的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
下列应用不涉及氧化还原反应的是
| A.Na2O2用作呼吸面具的供氧剂 | B.工业上电解熔融状态Al2O3制备Al |
| C.工业上利用合成氨实现人工固氮 | D.实验室用NH4Cl 和Ca(OH)2制备NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关说法正确的是
| A.塑料垃圾可直接露天焚烧 |
| B.实施“禁塑令”有助于遏制白色污染 |
| C.纤维素、油脂、蛋白质均属于有机高分子 |
D.聚丙烯结构简式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
由中学化学常见元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转化关系,A是由地壳中含量最多的金属元素组成的。请回答:
(1)写出下列物质的化学式:乙_______、丁_______、戊_______
(2)写出甲物质在工业上的一种主要用途:_______
(3)写出甲→乙+丙反应的离子方程式:____________
A→乙+C反应的化学方程式______________
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
下表为部分短周期元素化合价及其相应原子半径的数据。请回答下列问题:
(1)元素G在周期中的位置是 ;元素F所形成的常见单质的电子式为 。
(2)A、B、C、E的氢化物稳定性顺序是 。(用化学式回答)
(3)分子组成为ACH2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是 。
(4)请写出B的单质的一种重要用途 ;工业上制取该单质的原理反应为 。
(5)请设计一个实验方案,使铜和A的最高价氧化物对应的水化物的稀溶液反应,得到蓝色溶液和氢气。请在方框内绘出该实验方案原理装置示意图。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
某铵态氮肥由W、X、Y、Z等4种短周期元素组成,其中W的原子半径最小。
I.若Y、Z同主族,ZY2是形成酸雨的主要物质之一。
(1)将X、Y、Z的元素符号填在右图所示元素周期表(局部)中的相应位置上。
(2)X的最髙价氧化物对应水化物的稀溶液与铜反应的化学方程式为___ ___。
(3)一定条件下,1mol XW3气体与O2完全反应生成X元素的单质和液态水,放出382.8 kJ热量。该反应的热化学方程式为________________________。
II.若Z是形成化合物种类最多的元素。
(4)该氮肥的名称是______(填一种)。
(5)HR是含Z元素的一元酸。室温时,用0.250mol?L—1NaOH溶液滴定25.0 mL HR溶液时,溶液的pH变化情况如图所示。其中,a点表示两种物质恰好完全反应。
①右图中x______7(填“>”、“<”或“=”)。
②室温时,HR的电离常数Ka=______(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
已知短周期的主族元素X、Y、Z、W、M的原子序数依次增大,X 是常见化肥的主要元素,Y 原子的最外层只有2个电子,Z单质可制成半导体材料,W元素形成的单质为黄色的固体。请回答以下问题:
(1)元素W在周期表的位置为 ;
(2)X与Y形成的化合物的电子式 ;
(3)Z的氧化物晶体类型为 ,12gZ的氧化物中含有的共价键数为 ;
(4)X、W形成的氢化物分别为甲和乙,且甲、乙所含的电子数相等,则甲的结构式为 ;
(5)W和M都是较活泼的非金属元素,用实验事实表明这两种元素的非金属性强弱 (用方程式书写或文字说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(12分)【化学——有机化学基础】
化合物Ⅲ具有水果香味,在实验室可通过如下反应制得: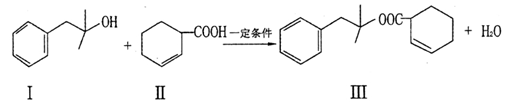
化合物I可通过下列路径合成:
(1)化合物Ⅱ能使Br2的CCl4溶液褪色,其反应化学方程式为 。
(2)化合物Ⅳ的结构简式为 ,生成化合物Ⅳ的反应类型为 。
(3)在浓硫酸和加热条件下,化合物I易发生消去反应生成含2个甲基的产物,该反应化学方程式为 。
(4)写出满足下列条件的化合物Ⅱ的三种同分异构体 、 、 。
①含一个六元环 ②无酸性,酸性条件下水解生成两种有机物 ③能发生银镜反应
(5)CH3CH2MgBr和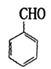 也能发生类似V
也能发生类似V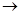 Ⅵ的反应,请写出所生成醇的结构简式 。
Ⅵ的反应,请写出所生成醇的结构简式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com