
铝是地壳中含量最多的金属元素,1854年法国化学家德维尔用金属钠还原氯化钠和氯化铝的复盐,获得了铝单质。1886年,美国人豪尔和法国人海郎特,分别独立地电解熔融的氧化铝和冰晶石的混合物,制得了金属铝,奠定了今天大规模生产铝的基础。
工业生产金属铝的原料是铝土矿(主要成分为Al2O3,另含有Fe2O3和SiO2),工业中得到较纯氧化铝的过程如下图所示:

试回答下列问题:
(1)操作Ⅰ是一种重要的混合物分离方法,实验室进行该项操作用到的玻璃仪器有烧杯、________、________。
(2)经分析不溶物A的主要成分为________。
(3)工业上电解冶炼铝的化学方程式为________________,若电路中通过1 mol电子,可以得到铝________g。
(4)为了提高综合经济效益,实际工业生产中常将上述反应中的相关物质循环利用。其部分转化关系如下图所示:

①上述转化中未涉及四种基本反应类型中的________反应;
②写出过程③的化学方程式:____________。
(5)科学研究表明,人体过量吸入铝元素会严重危害身体健康。请你结合实际提出两条杜绝铝元素过量吸入的措施:____________。
(1)漏斗 玻璃棒
(2)Fe2O3和SiO2(提示:Fe2O3不溶于水,且不与NaOH溶液反应;SiO2属于原子晶体,常温下与NaOH反应的速率很慢)
(3)2Al2O3 4Al+3O2↑ 9
4Al+3O2↑ 9
(4)①置换 ②NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
(5)不用铝制品作炊具;不用铝箔包装食品(其他合理答案也可)
【解析】本题考查工业提取铝的流程实验。铝土矿加碱溶解后,溶液A为NaAlO2,不溶物为Fe2O3和SiO2,在NaAlO2溶液中通入CO2可生成Al(OH)3和NaHCO3,Al(OH)3受热分解生成Al2O3,Al2O3电解产生金属铝,方程式为2Al2O3 4Al+3O2↑,该反应中产生4 mol铝需要转移电子为12 mol,则转移1 mol电子可以得到铝
4Al+3O2↑,该反应中产生4 mol铝需要转移电子为12 mol,则转移1 mol电子可以得到铝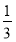 mol,即为9 g;(4)B为NaHCO3,根据题意可知,物质X为CaCO3,高温分解产生CaO和CO2,CaO与水反应生成Ca(OH)2,Ca(OH)2与NaHCO3反应生成NaOH和CaCO3,反应①为分解反应,反应②为化合反应,反应③为复分解反应。
mol,即为9 g;(4)B为NaHCO3,根据题意可知,物质X为CaCO3,高温分解产生CaO和CO2,CaO与水反应生成Ca(OH)2,Ca(OH)2与NaHCO3反应生成NaOH和CaCO3,反应①为分解反应,反应②为化合反应,反应③为复分解反应。


科目:高中化学 来源:2014高考化学二轮复习限时集训 专题3氧化还原反应练习卷(解析版) 题型:选择题
下列各种转化不符合实质上“一定是被氧化”的是( )
A.氮的固定 B.钢铁的腐蚀 C.食物的腐败 D.铁或铝在浓硫酸中的钝化
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 3.2合成洗涤剂的生产练习卷(解析版) 题型:选择题
下列产品的使用不会对环境造成污染的是( )。
A.含磷洗衣粉 B.酒精 C.氟利昂 D.含汞电池
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 2专题综合检测练习卷(解析版) 题型:选择题
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
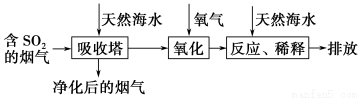
下列说法错误的是( )。
A.天然海水pH≈8的原因是海水中的CO32-、HCO3-水解
B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42-
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸
D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 2专题综合检测练习卷(解析版) 题型:选择题
下列废物处理方法中正确的是( )。
A.化学实验中产生的二氧化硫废气可用浓硫酸吸收
B.化学实验中产生的二氧化氮废气可用水直接吸收
C.用黄铁矿作原料生产硫酸的过程中产生的废渣可用于提取燃料
D.用黄铁矿作原料生产硫酸的过程中产生的废气可用于提取漂白剂
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 2.4镁和铝的冶炼练习卷(解析版) 题型:选择题
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是 ( )。
A.②④⑤③① B.③②④①⑤
C.③④②⑤① D.②④③⑤①
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 2.3硫酸工业练习卷(解析版) 题型:选择题
有关接触法制硫酸的叙述不正确的是( )。
A.硫磺和硫铁矿均可作为生产原料
B.将矿石粉碎,是为了提高矿石的利用率
C.反应中通入过量的空气是为了提高FeS2和SO2的转化率
D.从吸收塔出来的硫酸经浓缩后可以变成发烟硫酸
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 1专题综合检测练习卷(解析版) 题型:选择题
铁酸钠(Na2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe3+。
(1)铁酸钠中铁元素的化合价为________。铁酸钠能消毒杀菌,这是因为它具有________性。
(2)铁酸钠用于水处理时,除了能消毒杀菌外,还能沉降水中的悬浮杂质,起到净水作用,请说明其净水原理__________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 8化学平衡移动练习卷(解析版) 题型:选择题
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
气体体积/L c(Y)/(mol·L-1) 温度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是( )
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减小
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com