
| A. | 新制饱和氯水中:Na+、Al3+、SO32-、SO42- | |
| B. | 加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- | |
| C. | 常温下,在碱性的溶液中:K+、AlO2-、CO32-、Na+ | |
| D. | 在碱性的溶液中:K+、NH4+、AlO2-、HCO3- |
分析 A.饱和氯水能够氧化亚硫酸根离子,亚硫酸根离子与铝离子发生双水解反应;
B.加入铝粉能产生氢气的溶液中存在大量氢离子或氢氧根离子,铵根离子、亚铁离子与氢氧根离子反应,硝酸根离子在酸性条件下能够氧化亚铁离子;
C.四种离子之间不反应,都不与碱性溶液中的氢氧根离子反应;
D.铵根离子、碳酸氢根离子与碱性溶液中的氢氧根离子反应,碳酸氢根离子的酸性大于氢氧化铝,能够与偏铝酸根离子反应生成氢氧化铝沉淀.
解答 解:A.Al3+、SO32-之间发生双水解反应,饱和氯水能够氧化SO32-,在溶液中不能大量共存,故A错误;
B.加入铝粉能产生氢气的溶液为酸性或强碱性溶液,NH4+与氢氧根离子反应,Fe2+、NO3-在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故B错误;
C.碱性溶液中存在大量氢氧根离子,K+、AlO2-、CO32-、Na+之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.碱性溶液中存在大量氢氧根离子,NH4+、HCO3-与氢氧根离子反应,AlO2-、HCO3-之间反应生成氢氧化铝沉淀和碳酸根离子,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源: 题型:选择题
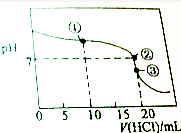 常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )
常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )| A. | 该氨水的浓度0.1000mol•L-1 | |
| B. | 点①溶液中c(NH4+)+c(NH3•H2O)+c(NH3)=2c(Cl-) | |
| C. | 点②溶液中c(NH4+)=c(Cl-) | |
| D. | 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
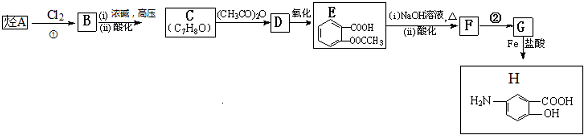
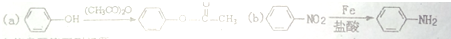
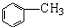 ,F含有的官能团是羧基和酚羟基(填名称).
,F含有的官能团是羧基和酚羟基(填名称).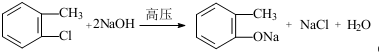 .
.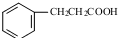 .
.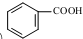 发生取代时,在羧基间位取代;②
发生取代时,在羧基间位取代;②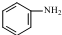 易发生氧化反应.以A为原料合成化合物
易发生氧化反应.以A为原料合成化合物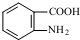 的设计合成路线为(其他试剂任选):
的设计合成路线为(其他试剂任选):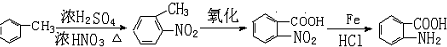 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:A>C>B>D | B. | 原子半径:B>D>C>A | ||
| C. | 原子序数:C>B>D>A | D. | 简单离子半径:D>B>C>A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
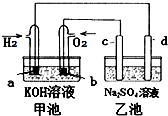 如图用氢氧燃料电池电解硫酸钠溶液(均为惰性电极),下列说法正确的是( )
如图用氢氧燃料电池电解硫酸钠溶液(均为惰性电极),下列说法正确的是( )| 甲池 | 乙池 | |
| A | 放电过程中KOH浓度不变 | 滴加酚酞试液d极区域溶液先变红 |
| B | OH-移向a电极 | OH-移向d电极 |
| C | a电极消耗2.24LH2时 (标准状况) | c电极生成1.12LO2 (标准状况) |
| D | a电极反应:H2-2e-=2H+ | d电极反应:4OH--4e-=O2↑+2H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
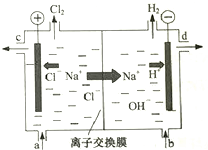 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
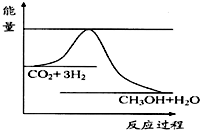 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com