
【题目】某硫原子的质量是ag,12C原子的质量是bg,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是( )
①该硫原子的相对原子质量为![]() ②mg该硫原子的物质的量为
②mg该硫原子的物质的量为![]() mol
mol
③该硫原子的摩尔质量是aNA g ④ag该硫原子所含的电子数为16NA
A. ①③ B. ②④ C. ①② D. ②③
科目:高中化学 来源: 题型:
【题目】燃煤及工业废气中的SO2是形成酸雨的主要原因,消除SO2是减少酸雨形成的有效方法。完成下列问题:
(1)已知:4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g)△H=﹣3412.0kJmol﹣1
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=﹣25.0 kJmol﹣1
2C(s)+O2(g)═2CO(g)△H=﹣221.0 kJmol﹣1
则2FeS2(s)+7O2(g)+3C(s)═2Fe(s)+3CO2(g)+4SO2(g)△H=_____kJmol﹣1。
(2)碱性NaClO2溶液脱硫法
SO2与碱性NaClO2溶液反应的离子方程式为2SO2+ClO2﹣+4OH﹣2SO42﹣+C1﹣+2H2O,已知pc=﹣lgc(SO2)。在刚性容器中,将含SO2的废气通入碱性NaClO2溶液中,测得pc与温度的关系如图所示。
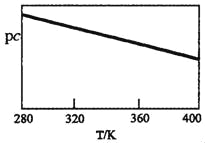
由图分析可知,该脱硫反应是_____反应(填“放热”或“吸热”);若温度不变,增大压强,该脱硫反应的平衡常数K_____(填“增大”、“减小”或“不变”)。
(3)燃料细菌脱硫法
①含FeS2的燃煤可用氧化亚铁硫杆菌(T.f)、氧化亚铁微螺菌(L.f)、氧化硫硫杆菌(T.t)进行脱硫,其脱硫过程如图所示:
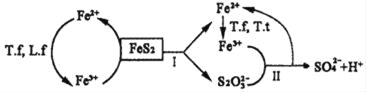
已知:脱硫总反应为:FeS2+14Fe3++8H2O═2SO42﹣+15Fe2++16H+,
Ⅰ反应的化学方程式为:FeS2+6Fe3++3H2O═S2O32﹣+7Fe2++6H+;
写出Ⅱ反应的化学方程式_____。
②在上述脱硫反应中,氧化亚铁硫杆菌(T.f)与Fe3+的形成过程可视为下图所示的原电池:

该细胞膜为_____(填“阳离子交换膜”或“阴离子交换膜”)。该电池的正极电极反应式为_____。该方法在高温下脱硫效率大大降低,原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2p轨道上最多只能排布6个电子,其依据的规律是__________________。
(2)氧元素基态原子核外未成对电子数为________个,第三周期中有两个成单电子的元素符号________(填一种即可),M层上有2对成对电子的原子最外层共有________种不同运动状态的电子。
(3)1~36号元素原子中未成对电子数为2的元素符号及价电子排布式________________。
(4)X元素的价电子排布式是4s24p5,X元素的符号是________。
(5)某元素的原子序数为33,该元素原子的价电子排布式为________,该元素原子核外有________个电子层,________个能级,________个原子轨道。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的混合气体在密闭容器中发生反应 mA(g)+nB(g)![]() pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/3,达到平衡时,C的浓度为原来的2.5倍,则下列说法正确的是
pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/3,达到平衡时,C的浓度为原来的2.5倍,则下列说法正确的是
A. C的体积分数增加 B. A的转化率降低
C. 平衡向正反应方向移动 D. m+n>p
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
新型储氢材料是氢能的重要研究方向。
(1)化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。
①基态O原子的电子占据了___________个能层,最高能级有___________种运动状态不同的电子。
②CH4、H2O、CO2分子键角从大到小的顺序是___________。生成物H3BNH3中是否存在配位键___________(填“是”或“否”)。
(2)掺杂T基催化剂的NaAlH4是其中一种具有较好吸、放氢性能的可逆储氢材料。NaAlH4由Na+和AlH4-构成,与AlH4-互为等电子体的分子有____(任写一个),Al原子的杂化轨道类型是____。Na、Al、H元素的电负性由大到小的顺序为_____。
(3)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。

①该晶体的化学式为___________。
②已知该晶胞的摩尔质量为Mg/mol,密度为dg/cm3。设NA为阿伏加徳罗常数的值,则该晶胞的体积是___________cm3(用含M、d、NA的代数式表示)。
③已知晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较温定,晶胞参数分别为apm、apm、cpm。标准状况下氢气的密度为Mg/cm3;若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为___________。(用相关字母表示已知储氢能力=![]() )。
)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液中离子关系的说法正确的是( )
A. 0.1 mol·L-1NaHCO3溶液中离子浓度关系:c(Na+)=2c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
B. 把0.2 mol/L NH4Cl溶液与0.1 mol/L NaOH溶液等体积混合后离子浓度关系:c(Cl-)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
C. 常温,向醋酸钠溶液中滴加少量醋酸使其pH=7,则混合液中:c(Na+)=c(CH3COO-)
D. 在Na2CO3溶液中,c(H+)+c(![]() )+c(H2CO3)= c(OH-)
)+c(H2CO3)= c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的溶液在蒸发皿中加热蒸干并灼烧,可以得到该物质本身的是( )
①CuSO4;②KHCO3;③FeSO4;④NH4Cl;⑤MgSO4;⑥AlCl3 ;
A. ①③ B. ①⑤ C. ①③⑤ D. ①②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体是日常生活中的一种混合物。
(1)下列有关胶体的说法中,不正确的是(___________)
A. 胶体、溶液、浊液的分类依据是分散质微粒直径大小
B. “卤水点豆腐”、“黄河入海口处的沙洲”都与胶体的聚沉有关
C. 向1 mol/L氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体
D. 可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体
(2)在水泥和冶金工业常用高压电对气溶胶作用除去大量烟尘,以减少对空气的污染,这种做法应用的原理是______。
(3)某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
①写出制备Fe(OH)3胶体的化学反应方程式:________。
②取少量制得的胶体加入试管中,再加入少量饱和氯化钠溶液,观察到的现象____,这种现象称为胶体的____。
③![]() 胶体能稳定存在的主要原因是____________。
胶体能稳定存在的主要原因是____________。
A.胶粒直径小于1nm B.胶粒带正电荷 C.胶粒作布朗运动 D.胶粒能透过滤纸
(4)有关制备Fe(OH)3胶体实验方案评价。某同学在制备Fe(OH)3胶体时将蒸馏水改为自来水煮沸后进行实验,该同学是否能得到胶体?______,(能或不能)理由_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. 常温下,反应C(s)+CO2(g)===2CO(g)不能自发进行,则该反应的ΔH>0
D. 同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com