
准确配制某体积的0.25 mol/L的NaOH溶液,试回答下列问题:
(1)A学生准确计算出需要NaOH固体的质量为5.0 g ,实验所用仪器中的定量仪器除了天平、量筒和烧杯以外,另一个重要的定量仪器是 。
(2) 配制方法:某同学设计了四个操作步骤:
①向盛有NaOH的烧杯中加入200 mL蒸馏水使其溶解,并冷却至室温。
②将NaOH溶液沿玻璃棒注入500 mL容量瓶中。
③继续往容量瓶中加蒸馏水至液面接近刻度线1~2 cm。
④改用 (填仪器名称)加蒸馏水至液面与刻度线相切,加盖摇匀。
若按上述步骤配制溶液物质的量浓度会________(填“偏高”或“偏低”或“无影响”)。若无影响下面不用填写,若有影响,应在步骤________________之间,补充的操作是__________________________________________________________________________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
 酸碱中和反应是中学化学一类重要的反应,某学生实验小组对课本中的两个酸碱中和实验进行了研究.
酸碱中和反应是中学化学一类重要的反应,某学生实验小组对课本中的两个酸碱中和实验进行了研究.| 实验次数 | 起始滴定管读数 | 终点滴定管读数 |
| 1 | 0.00mL | 24.02mL |
| 2 | 0.50mL | 24.46mL |
| 3 | 2.50mL | 25.02mL |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
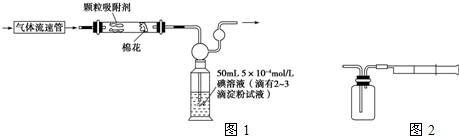
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
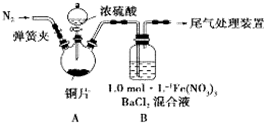 我省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,汽油中的硫含量下降三分之二,对二氧化硫的排放有了大大的改善,SO2可以用Fe( NO3)3溶液吸收,某化学兴趣小组对SO2和 Fe( NO3)3 溶液的反应[0.1mol/L的Fe(NO3)3 溶液的 pH=2]做了相应探究.
我省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,汽油中的硫含量下降三分之二,对二氧化硫的排放有了大大的改善,SO2可以用Fe( NO3)3溶液吸收,某化学兴趣小组对SO2和 Fe( NO3)3 溶液的反应[0.1mol/L的Fe(NO3)3 溶液的 pH=2]做了相应探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com