
| Cu |
| △ |
| Cu |
| △ |


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
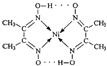 分子内的作用力除共价键外,还存在的两种作用力是
分子内的作用力除共价键外,还存在的两种作用力是 、④HCHO等,其中碳原子采取sp2杂化的分子有
、④HCHO等,其中碳原子采取sp2杂化的分子有
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、晶体硅是通信工程中制作光导纤维的主要原料,Na2SiO3常用来作木材防火剂. |
| B、漂白液是将氯气通入冷的消石灰[Ca(OH)2]中制得的,其有效成分为Ca(ClO)2 |
| C、酸雨是由于氮的氧化物和硫的氧化物的大量排放引起的,其中pH<5.6的为酸雨 |
| D、胃酸过多的病人可以服用氢氧化铝或者苏打来中和胃酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④ | B、②③ | C、①③ | D、②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com