
【题目】如图是一套实验室制取乙烯并验证乙烯具有还原性的实验装置。

请回答:
(1)实验步骤
①__________________________________;
②在各装置中注入相应的试剂(如图所示);
③______________________________;实验时烧瓶中液体混合物逐渐变黑。
(2)能够说明乙烯具有还原性的现象是_________________;装置甲的作用是_________________。若无甲装置,是否也能检验乙烯具有还原性,简述其理由:_________________。
【答案】(1)①组装仪器,检验装置的气密性 ③加热,使温度迅速升到170℃(2)乙中酸性KMnO4溶液紫色褪去 除去乙烯中混有的SO2、CO2等酸性气体 不能,因SO2具有还原性,也可以使酸性KMnO4溶液褪色
【解析】(1)①制取气体的装置气密性必须良好,实验前需要检验装置的气密性。
②实验室制乙烯时应使反应混合物的温度迅速升到170℃,而减少乙醚的生成。
(2)乙烯具有还原性是根据氧化剂酸性KMnO4溶液褪色来判断的。由于烧瓶中混合物变黑,则说明生成了碳,联想浓H2SO2具有强氧化性,可知在乙烯中含有还原性气体SO2,由于SO2也会使酸性KMnO4溶液褪色,会干扰验证乙烯的还原性,所以检验乙烯的还原性前必须除净SO2,则装置甲的作用是除去SO2。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.
(1)一定温度下,向固定体积为2L的密闭容器中充入SO2和NO2各1mol,发生反应SO2(g)+NO2(g)SO3(g)+NO(g),测得上述反应5min末到达平衡,此时容器中NO与NO2的体积比为3:1,则这段时间内SO2的反应速率υ(SO2)= , 此反应在该温度下的平衡常数K= .
(2)甲醇日趋成为重要的有机燃料,通常利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示: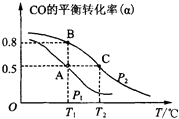
①上述合成甲醇的反应为反应(填“放热”或“吸热”).
②A、B、C三点的平衡常数KA、KB、KC的大小关系为 . A、B两点对应的压强大小关系是PAPB(填“大于”、“小于”或“等于”).
③若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为 , 理论上通过外电路的电子最多为 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人。这种做法的化学原因是( )
A. 胶体的电泳 B. 血液的氧化还原反应
C. 血液中发生复分解反应 D. 胶体的聚沉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下自发反应能用ΔH判据来解释的是( )
A. 硝酸铵自发地溶于水
B. 2N2O5(g)===4NO2(g)+O2(g) ΔH=+156.7 kJ·mol-1
C. (NH4)2CO3(s)===NH4HCO3(s)+NH3(g) ΔH=+74.9 kJ·mol-1
D. 2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2===CH2↑+H2O
CH2===CH2↑+H2O
CH2===CH2+Br2→BrCH2CH2Br
可能存在的副反应有乙醇在浓硫酸存在下140℃时脱水生成乙醚。
用少量的溴和足量的乙醇反应制备1,2二溴乙烷的装置如图所示:

乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
请回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度升高到170℃左右,最主要的目的是________(填序号,下同)。
a.引发反应
b.加快反应速度
c.防止乙醇挥发
d.减少副产物乙醚生成
(2)在装置C中应加入___________,其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸
c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是____________________。
(4)将1,2二溴乙烷粗产品置于分液漏斗中,加水振荡后静置,产物应在________(填“上”或“下”)层。
(5)若产物中有少量未反应的Br2,最好用________洗涤除去。
a.水 b.氢氧化钠溶液
c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用________的方法除去。
(7)反应过程中应用冷水冷却装置D,其主要目的是________________;但又不能过度冷却(如用冰水),其原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表达式正确的是( )
A.CH3COOH溶液中CH3COOH的电离:CH3COOH=H ++CH3COO﹣
B.用CuCl2溶液做导电实验,灯泡发光:CuCl2 ![]() Cu2++2Cl﹣
Cu2++2Cl﹣
C.NaHCO3溶液中HCO3﹣的水解:HCO3﹣+H2 O?H3 O ++CO32﹣
D.将FeCl3溶液滴入Na2CO3溶液中:2Fe3++3 CO32 ̄+3 H2 O═2Fe(OH)3↓+3 CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应3Fe(s)+4H2O(g)Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,保持压强不变,充入Ar,其正反应速率(A.变快 B.不变 C变慢,填字母代号);该反应向(填正移、逆移或不移).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作(或注意事项)中,主要是出于实验安全考虑的是
A.实验剩余的药品不能放回原试剂瓶 B.可燃性气体的验纯
C.气体实验装置在实验前进行气密性检查 D.滴管不能交叉使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个体积为1 L的密闭容器中发生某化学反应:2A(g)![]() B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800° C,实验Ⅲ在950°C。B、C的起始浓度都为0,反应物A的浓度(mol L-1)随时间(min)的变化如图所示。试回答下列问题:
B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800° C,实验Ⅲ在950°C。B、C的起始浓度都为0,反应物A的浓度(mol L-1)随时间(min)的变化如图所示。试回答下列问题:

(1)在实验Ⅰ中,反应在2040 min内A的平均反应速率为________mol L-1min-1。实验Ⅱ和实验Ⅰ相比,可能隐含的反应条件是____________。
(2)该反应的ΔH___________0,其判断理由是_____________。
(3)实验Ⅰ第40 min末,若降低反应温度,达到新的平衡后,A的浓度不可能为________(填序号)。
A.0.35 mol·L1 B.0.4 mol·L1 C.0.7 mol·L1 D.0.8 mol·L1
(4)若反应在800°C进行,在该1 L的密闭容器中加入1 mol A、0.2 mol He,达到平衡时A的转化率应____________。
A.等于86% B.等于50% C.小于50% D.在50%86%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com