
【题目】用NA 表示阿伏加德罗常数的数值, 则下列说法中正确的是( )
A. 44 g CO2所含质子数为28NA个
B. 常温常压下, 11.2 L氧气含原子数为NA个
C. 常温常压下, NA个氢分子的质量为1g
D. 2.3 g金属钠变为钠离子失去电子数为0.1NA
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】合成药物异搏定路线中某一步骤如下:

下列说法正确的是
A. 化合物Z可以发生取代、加成、氧化、加聚反应
B. 1mol化合物Y最多与1molNaOH发生反应
C. 化合物Y中所有原子可能在同一平面内
D. 可以用NaOH溶液检验化合物Z中有没有残留的化合物X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氧化还原反应中,水作为氧化剂的是
A. CO+H2O![]() CO2+H2 B. 3NO2+H2O=2HNO3+NO
CO2+H2 B. 3NO2+H2O=2HNO3+NO
C. 2Na2O2+2H2O=4NaOH+O2↑ D. 2F2+2H2O=4HF+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4===ZnSO4+H2↑,下列叙述正确的是( )
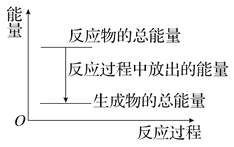
A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则锌作正极
D. 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法适合实验室制取氨气的是
A.N2和H2催化加热制取氨气
B.加热NH4HCO3制取氨气
C.将浓氨水向生石灰固体上滴加
D.将NH4Cl稀溶液和NaOH稀溶液混合
查看答案和解析>>
科目:高中化学 来源: 题型:
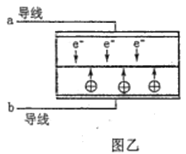
【题目】LED系列产品是一类新型节能产品。图甲是NaBH4/H2O2燃料电池的装置示意图,图乙是LED发光二极管的装置示意图。下列叙述错误的是( )
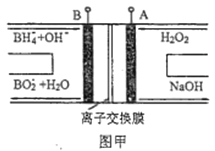
A. 电池应选用阳离子交换膜,Na+向A极区移动
B. 电池A极区的电极反应式为:H2O2+2e-=2OH-
C. 每有1molNaBH4参加反应,转移电子数为4NA
D. 要使LED发光二极管正常发光,图乙中的导线a应与图甲中的B极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g) ΔH=Q,2min末达到平衡,生成0.8 molD。
2C(g)+2D(g) ΔH=Q,2min末达到平衡,生成0.8 molD。
(1)300 ℃时,该反应的平衡常数表达式为:K=___________________。已知K300 ℃<K350 ℃,则ΔH ______0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。
(3)若温度不变,缩小容器容积,则A的转化率______(填“增大”“减小”或“变”)。
(4)如果在相同的条件下,上述反应从逆反应方向进行,开始时加入C、D各![]() mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B______mol。
mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素在周期表中的位置如图,则下列说法错误的是

A. 若Y的最简单氢化物的沸点比M的低,则X单质可与强碱溶液反应
B. 简单阴离子半径M>Z>Y
C. 若Y的氢化物水溶液呈碱性,则X的氧化物不与任何酸反应
D. 最高价氧化物对应水化物的酸性Z>M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com