
【题目】(1)含氢原子8g的CH4所含原子总数是标况下____升H2所含原子总数的二倍。
(2)标况下,W g CO2与4.48 LH2的混合气体的总体积等于32g CH4的体积,求W=___。
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态 Cl原子核外电子排布式__________________________,P、S、Cl的第一电离能由大到小顺序
为____________________。
(2)SCl2分子中的中心原子杂化轨道类型是_____________,该分子构型为__________。
(3)Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为__________。
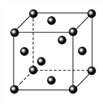
(4)已知MgO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66 pm和69 pm。则熔点:MgO_____NiO(填“>”、“<”或“=”),理由是_____________。

(5)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为______。
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+ 填充其中(如图2),已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为______g。(用a、NA表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素。稀土元素有“工业维生素”的美称,如今已成为极其重要的战略资源。
(1)钪(Sc)为21号元素,位于周期表的_____区,基态原子价电子排布图为_______。
(2)离子化合物Na3[Sc(OH)6]中,存在的化学键除离子键外还有_______。
(3)Sm(钐)的单质与l,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+CH2=CH2。ICH2CH2I中碳原子杂化轨道类型为______, lmol CH2=CH2中含有的σ键数目为______。常温下l,2-二碘乙烷为液体而乙烷为气体,其主要原因是__________
(4)与N3-互为等电子体的分子有________________(写两个化学式)。
(5)Ce(铈)单质为面心立方晶体,其晶胞参数a=516pm。晶胞中Ce(铈)原子的配位数为_______,列式表示Ce(铈)单质的密度:________g/cm3(用NA表示阿伏伽德罗常数的值,不必计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 都属于多环烃类,下列有关它们的说法错误的是
都属于多环烃类,下列有关它们的说法错误的是
A. 这三种有机物的二氯代物同分异构体数目相同
B. 盘烯能使酸性高锰酸钾溶液褪色
C. 棱晶烷和盘烯互为同分异构体
D. 等质量的这三种有机物完全燃烧,耗氧量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的离子方程式。
(1)向Na2S2O3溶液中加入稀硫酸_____________________________________________________________
(2)在Mg(OH)2悬浊液中加入FeCl3溶液,沉淀变为红褐色____________________________________
(3)Mg(OH)2沉淀溶于NH4Cl溶液中______________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。

(1)写出装置甲的电解总反应方程式________________________________________。
(2)为完成上述实验,正确的连接顺序为E→_________________(填写连接的字母)。
(3)对硬质玻璃管里的氧化铜粉末进行加热前,需要先通一段时间某气体并检验该气体的纯度,检验该气体已经纯的具体的操作和现象为_______________________________。
(4)乙装置的a瓶溶液可选用__________________。
A.淀粉碘化钾溶液 B.酸性高锰酸钾溶液 C.硫化钠溶液 D.Fe(NO3)2溶液
(5)若a瓶中盛放过量的NaHSO3溶液,写出发生的离子反应方程式_____________________。
(6)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案。精确测量硬质玻璃管的质量为a g,加入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后:
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
乙方案不足之处是________________________________________________________。
按甲方案进行计算,Cu的相对原子质量为__________。(用含a、b、c的式子来表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是( )
A. 苯与硝酸反应制取硝基苯
B. 乙烯与氯化氢反应制取氯乙烷
C. 乙醇与钠反应生成乙醇钠
D. 油脂在酸性条件下生成甘油和高级脂肪酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1![]() 醋酸溶液的
醋酸溶液的![]() ,下列能使溶液
,下列能使溶液![]() 的措施是( )
的措施是( )
A. 将溶液稀释到原体积的10倍 B. 加入适量的醋酸钠固体
C. 加入等体积0.2![]() 盐酸 D. 提高溶液的温度
盐酸 D. 提高溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A. 0.1molH218O与D2O的混合物中所含中子数为NA
B. 17g羟基所含电子的数目为10NA
C. lLpH=l的H2SO4溶液中含有的H+数目为0.2NA
D. 密闭容器中1molH2(g)与1molI2(g)共热反应制备HI增加2NA个H-I键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com