
海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如下:
(1)可以用淀粉-KI试纸检验操作I中是否有溴生成,其操作方法是___________________。
(2)操作Ⅱ发生反应的离子方程式为_____________;可以用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和-1价,操作Ⅲ中如果用稀硫酸代替氯气,则操作Ⅲ中发生反应的离子方程式为______。
(3)溴苯是一种化工原料,可以用溴和苯反应合成。实验室合成溴苯的装置示意图如下:

下表为苯、溴和溴苯的相关数据:
| | 苯 | 溴 | 溴苯 |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)取一小块淀粉-KI试纸于玻璃片上,用玻璃棒蘸取待测液滴在试纸上,如果试纸变蓝,说明有溴生成,如果不变蓝,说明没有溴生成(2分,操作过程1分,结论1分。)
(2)SO2+Br2+2H2O=SO4-+2Br-+4H+; BrO3?+5Br?+6H+=3Br2+3H2O
(4)①分液漏斗(1分);c(不填编号不得分)
②C2,156℃(每空1分)
③溴、溴化氢、苯(3分,每少或错1种扣1分)
④不合理(1分),溴可以和NaOH溶液反应生成溴离子,也能产生浅黄色沉淀,无法确定是否生成溴化氢,即无法确定两者发生的是取代反应(要点一:溴和NaOH反应;要点二:无法确定是否生成溴化氢。少一个要点扣1分。)
解析试题分析:(1)若有溴生成,则能与淀粉-KI反应,Br2与KI置换出的I2能使淀粉变蓝,所以检验方法为:取一小块淀粉-KI试纸于玻璃片上,用玻璃棒蘸取待测液滴在试纸上,如果试纸变蓝,说明有溴生成,如果不变蓝,说明没有溴生成.
(2)操作Ⅱ发生反应Br2与SO2、H2O发生氧化还原反应,生成H2SO4和HBr,离子方程式为:SO2+Br2+2H2O=SO4-+2Br-+4H+;生成物中溴的化合价分别为+5和-1价,分别为NaBrO3、NaBr,操作Ⅲ中在稀硫酸存在的条件下,NaBrO3与NaBr发生氧化还原反应生成Br2,离子方程式为:BrO3?+5Br?+6H+=3Br2+3H2O
(4)①根据实验装置图,仪器B为分液漏斗; 该实验A装置液体体积一般不超过容积的2/3,不少于1/3,本实验所加液体反应物的体积为38.0mL,所以A的容积最适合的,100mL,C项正确。
②因为C1测量的是溶液的温度,C2测量的是蒸汽的温度,收集馏分时应测量蒸汽的温度,所以根据C2显示的温度,溴苯的沸点为156℃,因此C2显示的温度为156℃。
③溴、溴化氢、苯的沸点低于溴苯,所以收集溴苯之前,F装置承接的物质有溴、溴化氢、苯。
④因为溴和苯反应合成溴苯的反应,一般会有Br2剩余,Br2与NaOH反应生成NaBr,也能与AgNO3反应生成浅黄色沉淀,无法确定是否生成了溴化氢,所以该实验方案不合理。
考点:本题考查基本仪器和基本操作、离子方程式的书写、实验方案的分析。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
(18分)Na2S2O3是重要的化工原料,易溶于水。在中性或碱性环境中稳定。
I.制备Na2S2O3?5H2O
反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水。另取5g研细的硫粉,用3ml 乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3?5H2O,经过滤,洗涤,干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是 。
(2)仪器a的名称是 ,其作用是 。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是 ,检验是否存在该杂质的方法是 。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:
。
II.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol?L?1碘的标准溶液滴定。
反应原理为:2S2O32?+I2=S4O62-+2I?
(5)滴定至终点时,溶液颜色的变化: 。
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL。产品的纯度为(设Na2S2O3?5H2O相对分子质量为M) 。
III.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42?,常用作脱氧剂,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
生铁中含碳和硫等元素。化学兴趣小组对某生铁样品进行了探究。根据要求回答下列问题。
Ⅰ.生铁中碳和硫元素的定性检验
按如图装置进行实验(夹持仪器已略去,填接口字母代号)可以实现碳和硫元素的检验。
(1)仪器X的名称是 ;装置③⑤中试剂相同,装置④中盛放的试剂是 。(2)写出甲中反应的化学方程式 。(3)如果撤除装置③④⑤,能否确认生铁样品中碳元素的存在? ,理由是 。Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量。称取样品w1 g进行实验,充分反应后,测得装置⑥中生成的沉淀为w2 g,该样品中碳的质量分数为 (用含w1、w2的式子表示)。(5)乙同学认为,待一定量样品充分反应后,向装置④中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案测得的结果 (填“偏大”或“偏小”);若要提高硫元素含量的测定精度,在不改变实验原理的前提下,可以采取的一种措施是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室制取乙酸丁酯的实验装置有如下图所示两种装置供选用。其有关物质的物理性质如下表: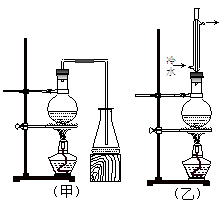
| | 乙酸 | 1-丁醇 | 乙酸丁酯 |
| 熔点(℃) | 16.6 | -89.5 | -73.5 |
| 沸点(℃) | 117.9 | 117 | 126.3 |
| 密度(g/cm3) | 1.05 | 0.81 | 0.88 |
| 水溶性 | 互溶 | 可溶(9g/100g水) | 微溶 |
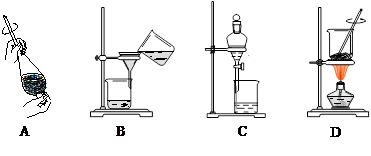
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下表:
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
|


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
已知某酸性土壤浸取液中除Fe3+外,还含有一定量Mg2+和Al3+。请设计合理实验检验该浸取液中的Mg2+、Al3+。
限选实验用品与试剂;烧杯、试管、玻璃棒、滴管、玻璃片、pH试纸;浸取液、20%KSCN、0.1 mol·L-1 NaOH、6 mol·L-1 NaOH、0.1 mol·L-1 HCl、蒸馏水。
必要时可参考:
| 沉淀物 | 开始沉淀时的pH | 沉淀完全时的pH |
| Mg(OH)2 | 9.6 | 11.1 |
| Fe(OH)3 | 2.7 | 3.7 |
| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: | |
| …… | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室可用MnO2和KClO3混合加热的方法制取氧气:2KClO3 2KCl+3O2↑
2KCl+3O2↑
I.现有下列仪器或装置:
(1)A-D装置中,用作KClO3为原料制氧气的反应装置是____(填序号)。
(2)排水法收集氧气,接口顺序是:氧气出口→___→___→g→h→烧杯(填序号)。
Ⅱ.KClO3分解时尚有副反应,导致收集到的气体有异味。据推测,副产物可能是O3、Cl2、ClO2中的一种或几种。资料表明:O3、Cl2、ClO2的沸点依次为-111℃、-34℃和11℃,且O3、ClO2也能将KI氧化为I2。为探究副反应气体产物的成分,将KClO3分解产生的气体经干燥后通入如右装置进行实验:
(3)若要确认副产物中含Cl2,F中应盛放_____溶液。
(4)确定副产物中含有ClO2的现象是_________________。
(5)实验时若D中无现象,E中试纸变蓝,能否得出副产物含有臭氧的结论?
答:_____ (填“能”或“不能”)。理由是________________________________。
Ⅲ.ClO2是饮用水消毒剂。用ClO2处理过的饮用水(pH为5.5~6.5)除含有ClO2外,常含有一定量对人体不利的ClO2-。为测定此饮用水中两者成分,进行如下实验:准确量取v mL水样加入到锥形瓶中,调节水样pH=8,加人足量KI晶体,发生如下反应:2ClO2+2I- =I2+2ClO2-,反应结束后产生amolI2;继续调节溶液pH=1,又发生如下反应:ClO2-+4H++4I- =2I2+Cl-+2H2O,反应结束后叉产生bmolI2。
(6)饮用水中c(ClO2-)=_____________mol·L- 1(用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
环己酮是一种重要的有机化工原料。实验室合成环己酮的反应如下: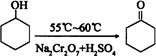
环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g·cm—3、20 ℃) | 溶解性 | |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 | |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 | |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO3·3H2O2),它具有杀菌消毒去油污的能力且不会污染水源。
(1)检验这种新型洗涤剂中金属阳离子的操作和现象是_______________________________________。
(2)这种洗涤剂中的双氧水可以将废水中的氰化物转化为无毒物同时生成NH3,写出反应的离子方程式:___________________________________
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用。试分析其中的原因(用离子方程式和简要文字表述):__________________________________________________________________
(4)某化学学习小组为定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤剂100 mL,加入25 gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.10 mol·L-1 NaOH溶液、8.0 mol·L-1 NaOH溶液、澄清石灰水、0.01 mol·L-1 KMnO4溶液、BaCl2稀溶液、品红溶液、蒸馏水、小木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2;
假设2:气体是________________;
假设3:气体是CO2。
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象与结论。
| 实验步骤 | 预期现象与结论 |
| 将气体依次通入盛有________、________的洗气瓶中,________ | __________________ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com