
(15分)
(1).CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式)。
(2).人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”。Ti 元素在元素周期表中的位置是 周期,第 族;其基态原子的价电子层排布为 ;
(3). 在Ti的化合物中,可以呈现+2、+3、+4 三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如图,它的化学式是 ;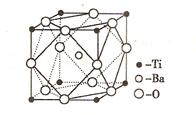
(4)已知Ti3+可形成配位数为6的配合物。现有含钛的两种颜色的晶体,一种为紫色,另一为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a. 分别取等质量的两种配合物晶体的样品配成待测溶液;
b. 分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c. 沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的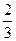 。
。
则绿色晶体配合物的化学式为 ,绿色晶体中含有化学键类型是 。
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
a b
c
观察上述结构,判断a中碳原子的杂化方式为 ,b对应的物质是 ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为 。
(2)在C60单质中,微粒之间的作用力为 ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为 ;写出另一与CO互为等电子体的化学式 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4 的结构为 ;写出基态Ni原子的电子排布式 。
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能 ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省海门市高二下学期期末教学质量调研化学试题 题型:填空题
碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
a  b
b  c
c 
观察上述结构,判断a中碳原子的杂化方式为 ,b对应的物质是 ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为 。
(2)在C60单质中,微粒之间的作用力为 ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为 ;写出另一与CO互为等电子体的化学式 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4的结构为 ;写出基态Ni原子的电子排布式 。
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特 点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能 ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是 。
查看答案和解析>>
科目:高中化学 来源:09—10年泰州中学高二下学期期末考试化学卷 题型:填空题
(8分)到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源。
请回答下列问题:
⑴2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2599kJ·mol-1,
则乙炔的燃烧热为 ▲ 。
⑵有些反应进行得很慢,有些反应不容易直接发生,有些反应的产品不纯(有副反应发生),这给测定反应热造成了困难,此时可利用盖斯定律,就可以间接地把它们的反应热计算出来。已知
①CO(g)+1/2O2(g)=== CO2(g) ΔH1=-283.0kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH2=-393.5kJ·mol-1
则C(s)+1/2O2(g)="CO(g) " ΔH = ▲ 。
⑶从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。已知键能数据如下表。
| 化学键 | 键能(kJ/mol) | 化学键 | 键能(kJ/mol) |
| N≡N | 942 | H-O | 460 |
| N-H | 391 | O=O | 499 |
| H-H | 437 | | |
 2NH3 △H=a kJ·mol-1。试根据表中所列键能数据估算a的数值 ▲ 。
2NH3 △H=a kJ·mol-1。试根据表中所列键能数据估算a的数值 ▲ 。查看答案和解析>>
科目:高中化学 来源:2012届江苏省海门市高二下学期期末教学质量调研化学试题 题型:填空题
碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
a  b
b  c
c 
观察上述结构,判断a中碳原子的杂化方式为 ,b对应的物质是 ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为 。
(2)在C60单质中,微粒之间的作用力为 ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为 ;写出另一与CO互为等电子体的化学式 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4 的结构为 ;写出基态Ni原子的电子排布式 。
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。

(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能 ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com