
(10分)铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l、+2。已知Cu2O与稀硫酸反应,溶液呈蓝色。现向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol/L HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,消耗H2SO4的物质的量为
。
(4)若混合物中Cu的物质的量为n mol,则n的取值范围为 。
(5)科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。在加热条件下用液态肼(N2H4)还原新制Cu(OH )2可制备纳米级Cu2O,同时放出N2。当收集的N2体积为 3.36L(已换算为标准状况)时,可制备纳米级Cu2O的质量为 。
(10分,每空2分)
(1)3 Cu2O +14 H+ + 2 NO3-= 6 Cu2+ + 2 NO↑ + 7 H2O
(2)16 g (3)0.1 mol (4)0.05<n<0.15 (5)43.2
【解析】
试题分析:(1)氧化亚铜与硝酸反应生成硝酸铜、NO、水,离子方程式为3 Cu2O +14 H+ + 2 NO3-= 6 Cu2+ + 2 NO↑ + 7 H2O;
(2)2240mLNO的物质的量是0.1mol,原硝酸溶液中硝酸的物质的量是0.6mol,所以未被还原的硝酸的物质的量是0.6-0.1=0.5mol,说明溶液中硝酸铜的物质的量是0.25mol,则铜离子得物质的量是0.25mol,根据铜元素守恒,若用氢气还原上述混合物得到单质铜的物质的量也是0.25mol,其质量是16g;
(3)设原混合物中Cu2O的物质的量是xmol,根据得失电子守恒,失去电子的物质的量是0.1×2+2x×1=(0.2+2x)mol,得电子的物质的量是0.1×3=0.3mol,所以0.2+2x=0.3,x=0.05mol,混合物中Cu元素的总物质的量是0.25mol,所以CuO的物质的量是0.1mol,所以需要硫酸的物质的量是0.1mol;
(4)由Cu元素守恒可得:2×n(Cu2O)+n(CuO)+n=0.25mol,由氧化还原反应得失电子守恒可知:n×2+2×n(Cu2O)=0.1mol×3,
解之得:n(CuO)=n-0.05mol>0,
n(Cu2O)=0.15mol-n>0,
所以0.05mol<n<0.15mol;
(5)N2H4生成氮气化合价升高,氢氧化铜生成氧化亚铜Cu的化合价降低,生成氮气的物质的量是3.36L/22.4L/mol=0.15mol,设生成Cu2O的物质的量是xmol,则2x=0.15mol×4,所以x=0.3mol,则生成Cu2O的质量是0.3mol×144g/mol=43.2g。
考点:考查氧化还原反应的分析,固体混合物的计算


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:2015届福建省福州八市高二下学期期中考试化学试卷(解析版) 题型:选择题
为了防止热带鱼池中水藻的生长,需保持水中Cu2+的浓度约1.2×10-5 mol·L-1。为避免在每次换池水时溶液浓度的改变,可把适当的含铜化合物放在池底,其饱和溶液提供适当的Cu2+。已知CuS、Cu(OH)2、CuCO3的Ksp值依次为1.3×10-36、2.2×10-20、1.4×10-10,下列四种物质中,能满足池水浓度要求的是( )
A.CuSO4 B.CuCO3 C.Cu(OH)2 D.CuS
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三上学期第一次检测考试化学试卷(解析版) 题型:选择题
常温下,在溶液中可发生以下反应:① H++Z-+XO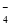 === X2++Z2+H2O(未配平),
=== X2++Z2+H2O(未配平),
② 2M2++R2===2M3++2R-,③ 2R-+Z2=== R2+2Z-。由此判断下列说法正确的是
A.常温下反应2M2++Z2===2M3 ++2Z-不可以自发进行
B.R元素在反应②中被氧化,在③中被还原
C.反应①配平后,H2O的化学计量数为8
D.还原性强弱顺序为:X2+>Z->R->M2+
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高三第一次模拟考试化学试卷(解析版)) 题型:选择题
在标准状况下,将V L A气体(摩尔质量M g/mol)溶于100ml水中(A与水不反应),所得A的水溶液密度为ρ g/cm3,则此溶液的物质的量浓度(mol/L)为( )
A.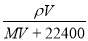 B.
B. 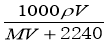 C.
C.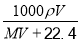 D.
D.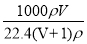
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高三第一次模拟考试化学试卷(解析版)) 题型:选择题
下列溶液中的Cl-物质的量与100ml 1 mol·L-1AlCl3溶液中Cl-相等的是( )
A.150ml 1 mol·L-1NaCl溶液 B.100ml 3mol·L-1KClO3溶液
C. 75ml 2 mol·L-1MgCl2溶液 D.50ml 1 mol·L-1FeCl3溶液
查看答案和解析>>
科目:高中化学 来源:2015届湖南省高三第一次月考化学试卷(解析版) 题型:选择题
质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为( )
A.大于2c mol/L B.等于2c mol/L
C.小于2c mol/L D.在c mol/L一2c mol/L之间
查看答案和解析>>
科目:高中化学 来源:2015届湖南省高三第一次月考化学试卷(解析版) 题型:选择题
V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO42-的物质的量浓度为( )
A.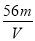 mol·L-1 B.
mol·L-1 B.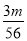 V mol·L-1 C.
V mol·L-1 C. V mol·L-1 D.
V mol·L-1 D.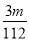 V mol·L-1
V mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高二下学期期中考试化学试卷(解析版) 题型:选择题
25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃8mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了18mL,原混合烃中乙炔的体积分数为( )
A.12.5% B.25% C.50% D.75%
查看答案和解析>>
科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
下列各组烃的混合物,只要总质量一定,按任意比例混合,完全燃烧后生成的CO2和H2O都是恒量的是( )
A.C2H2、C2H4 B.C2H4、C4H6 C.C2H6、C3H6 D.C6H6、C2H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com