
【题目】Ⅰ.在密闭容器中进行下列反应:CO2(g)+C(s)![]() 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡如何移动?(填“向左移动”、“向右移动”或“不移动”)
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡如何移动?(填“向左移动”、“向右移动”或“不移动”)
(1)增加C(s),平衡___。
(2)减小密闭容器容积,保持温度不变,则平衡___。
(3)通入N2,保持密闭容器容积和温度不变,则平衡__。
(4)保持密闭容器容积不变,升高温度,则平衡__。
Ⅱ.在一密闭容器中发生下列反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,如图是某一时间段反应速率与反应进程的关系曲线图。
2NH3(g) ΔH<0,如图是某一时间段反应速率与反应进程的关系曲线图。
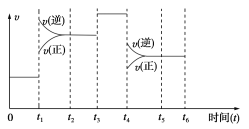
下列时间段中,氨的百分含量最高的是(_____)
A.0~t1 B.t2~t3
C.t3~t4 D.t4~t5
【答案】不移动 向左移动 不移动 向右移动 A
【解析】
Ⅰ.在密闭容器中进行下列反应:CO2(g)+C(s)![]() 2CO(g) ΔH>0,
2CO(g) ΔH>0,
此反应的特点是:反应物气体分子数小于生成物气体分子数,正反应为吸热反应。
(1)增加C(s),气体的浓度不变,平衡不受影响;
(2)减小密闭容器容积,也就是加压,保持温度不变,则平衡向气体分子数减小的方向移动;
(3)通入N2,保持密闭容器容积和温度不变,对气体的浓度不产生影响,平衡不受影响;
(4)保持密闭容器容积不变,升高温度,则平衡向吸热反应方向移动。
Ⅱ.从图中可以看出,两次改变条件,都是逆反应速率大,也就是平衡都逆向移动,氨的百分含量都在减小。
Ⅰ.在密闭容器中进行下列反应:CO2(g)+C(s)![]() 2CO(g) ΔH>0,
2CO(g) ΔH>0,
此反应的特点是:反应物气体分子数小于生成物气体分子数,正反应为吸热反应。
(1)增加C(s),但并未改变气体的浓度,平衡不受影响;答案为:不移动;
(2)减小密闭容器容积,也就是加压,保持温度不变,则平衡向气体分子数减小的方向移动,即向左移动;答案为:向左移动;
(3)通入N2,保持密闭容器容积和温度不变,对气体的浓度不产生影响,平衡不受影响;答案为:平衡不移动;
(4)保持密闭容器容积不变,升高温度,则平衡向吸热反应方向移动,即向右移动;答案为:向右移动。
Ⅱ.从图中可以看出,两次改变条件,都是逆反应速率大,也就是平衡都逆向移动,氨的百分含量都在减小,所以0~t1,氨的百分含量最高。答案为:0~t1。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的![]() 和较多的
和较多的![]() 和
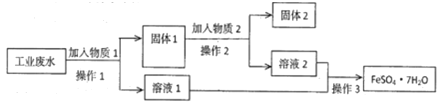
和![]() 为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
![]() 检验废水中的
检验废水中的![]() ,实验室中用酸性
,实验室中用酸性![]() 溶液检验,发生反应的离子方程式为______。
溶液检验,发生反应的离子方程式为______。
![]()
![]() 加入过量物质1后,发生反应的离子方程式为______。
加入过量物质1后,发生反应的离子方程式为______。
![]() 固体2是______,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入______。
固体2是______,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,互为同分异构体的是
A.CH3CH2CH3 和CH3CH(CH3)CH3B.CH3CH2OH 和 CH3CHO
C.CH3COOH 与 HCOOCH3D.![]() 和
和 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由一氯乙烷合成乙二醇的线路如下:
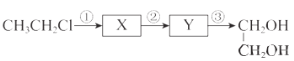
(1)反应①发生消去反应,反应试剂和条件为________________。
(2)反应②选用的无机试剂为_________________。
(3)反应③的化学方程式是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的![]() (如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关
(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关![]() 的说法正确的是
的说法正确的是

A. 分子中N、O间形成的共价键是非极性键
B. 分子中四个氮原子共平面
C. 该物质既有氧化性又有还原性
D. 15.2g该物资含有6.02×![]() 个原子
个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
元素 | 相关信息 |
Y | 原子核外有6个不同运动状态的电子 |
Z | 非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同 |
W | 主族元素,与Z原子的价电子数相同 |
R | 价层电子排布式为3d64s2 |
M | ⅠB族,其单质常用作导线 |
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是_____________________,M2+的核外电子排布式为________________________。
(2)写出两个与YZ2互为等电子体的化学式_________________ 。
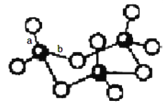
(3)WZ2分子中W原子价层电子对数是_____________对,WZ2的VSEPR 模型名称为_______________,WZ3气态为单分子,该分子中W原子的杂化轨道类型为__________________;WZ3的三聚体环状结构如图所示,该结构中W原子的杂化轨道类型为__________;该结构中W-Z键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为___________(填图中字母) ,该分子中含有______个σ键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数,下列说法正确的是( )
A. 标况下,11.2L氟化氢中含有的电子数5NA
B. 6.0g甲醛(HCHO)和醋酸的混合物中含有的原子总数为0.8NA
C. 100mL 0.1mol/L 的KAl(SO4)2溶液中含有的阳离子总数为0.02NA
D. 分别由H2O2和KMnO4制备等量的氧气转移的电子数目相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C10H18)→四氢萘(C10H12)→萘(C10H8)”的脱氢过程释放氢气。已知:
Ⅰ C10H18(l)==C10H12(l)+3H2(g) ΔH1 Ⅱ C10H12(l)==C10H8(l)+2H2(g) ΔH2
假设某温度下, ΔH1>ΔH2>0。在下图中绘制下列“C10H18→C10H12→C10H8”的“能量~反应过程” 示意图正确的是: ( )
A. 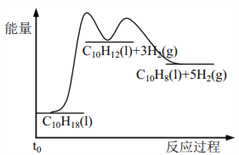 B.
B. 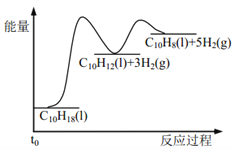
C. 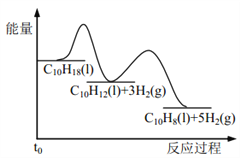 D.
D. 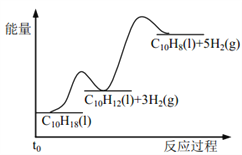
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1874年22岁的范特霍夫和27岁的勒贝尔分别提出碳正四面体学说,建立了分子的立体概念。如图所示均能表示甲烷的分子结构,哪一种更能反映其真实存在状况( )
A.结构示意图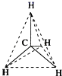 B.比例模型
B.比例模型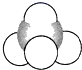
C.球棍模型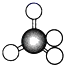 D.电子式
D.电子式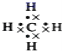
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com