
【题目】请写出下述过程各步的反应类型及化学方程式。
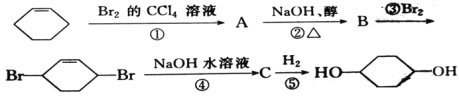
①为_____反应,化学方程式为________
②为_____反应,化学方程式为________
③为_____反应,化学方程式为________
④为_____反应,化学方程式为________
【答案】加成 ![]() + Br2→
+ Br2→![]() 消去
消去 ![]() + 2NaOH
+ 2NaOH![]()
![]() + 2NaBr +2H2O 加成
+ 2NaBr +2H2O 加成 ![]() + Br2→
+ Br2→![]() 水解(或取代)
水解(或取代) ![]() + 2NaOH
+ 2NaOH![]()
![]() + 2NaBr
+ 2NaBr
【解析】
环戊烯与溴加成生成A,A为![]() ,
,![]() 在氢氧化钠醇溶液中发生消去反应生成B。B为
在氢氧化钠醇溶液中发生消去反应生成B。B为![]() ,
,![]() 与溴发生1,4-加成反应生成
与溴发生1,4-加成反应生成![]() ,
,![]() 在氢氧化钠水溶液中发生水解反应生成C,C为
在氢氧化钠水溶液中发生水解反应生成C,C为![]() ,
,![]() 与氢气加成生成
与氢气加成生成![]() ,据此分析解答。
,据此分析解答。
①为环戊烯与溴的加成反应,化学方程式为![]() + Br2→
+ Br2→![]() ,②为
,②为![]() 在氢氧化钠醇溶液中发生消去反应,化学方程式为
在氢氧化钠醇溶液中发生消去反应,化学方程式为![]() + 2NaOH
+ 2NaOH![]()
![]() +2NaBr +2H2O,③为
+2NaBr +2H2O,③为![]() 与溴发生1,4-加成反应,化学方程式为
与溴发生1,4-加成反应,化学方程式为![]() + Br2→
+ Br2→![]() ,④为
,④为![]() 在氢氧化钠水溶液中发生水解反应,化学方程式为
在氢氧化钠水溶液中发生水解反应,化学方程式为![]() + 2NaOH
+ 2NaOH![]()
![]() + 2NaBr,故答案为:加成;
+ 2NaBr,故答案为:加成;![]() + Br2→
+ Br2→![]() ;消去;
;消去;![]() + 2NaOH
+ 2NaOH![]()
![]() + 2NaBr +2H2O;加成;
+ 2NaBr +2H2O;加成;![]() + Br2→
+ Br2→![]() ;水解(或取代);
;水解(或取代);![]() + 2NaOH
+ 2NaOH![]()
![]() + 2NaBr。
+ 2NaBr。


科目:高中化学 来源: 题型:
【题目】FeSO4 溶液放置在空气中容易变质,因此为了方便使用 Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)26H2O],它比绿矾或绿矾溶液更稳定。(稳定是指物质放置 在空气中不易发生各种化学反应而变质)
I.硫酸亚铁铵晶体的制备与检验
(1)某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都必须煮沸、冷却后再使用,这样处理蒸馏水的目的是_______。向 FeSO4 溶液中加入饱和(NH4)2SO4 溶液,经过操作_______、冷却结晶、过滤、洗涤和干燥后得到一 种浅蓝绿色的晶体。
(2)该小组同学继续设计实验证明所制得晶体的成分。
①如图所示实验的目的是_______,C 装置的作用是_______。
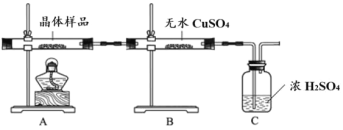
取少量晶体溶于水,得淡绿色待测液。
②取少量待测液,_______ (填操作与现象),证明所制得的晶体中有 Fe2+。
③取少量待测液,经其它实验证明晶体中有NH4+和SO42-
II.实验探究影响溶液中 Fe2+稳定性的因素
(3)配制 0.8 mol/L 的 FeSO4 溶液(pH=4.5)和 0.8 mol/L 的(NH4)2Fe(SO4)2 溶液(pH=4.0),各取 2 ml 上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加 2 滴 0.01mol/L 的 KSCN 溶液,15 分钟后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液;FeSO4溶液则出现淡黄色浑浊。
(资料 1)
沉淀 | Fe(OH)2 | Fe(OH)3 |
开始沉淀pH | 7.6 | 2.7 |
完全沉淀pH | 9.6 | 3.7 |
①请用离子方程式解释 FeSO4 溶液产生淡黄色浑浊的原因_______。
②讨论影响 Fe2+稳定性的因素,小组同学提出以下 3 种假设:
假设 1:其它条件相同时,NH4+的存在使(NH4)2Fe(SO4)2 溶液中 Fe2+稳定性较好。
假设 2:其它条件相同时,在一定 pH 范围内,溶液 pH 越小 Fe2+稳定性越好。
假设 3:_______。
(4)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分 别控制溶液 A(0.2 mol/L NaCl)和溶液 B(0.1mol/L FeSO4)为不同的 pH,

观察记录电流计读数,对假设 2 进行实验研究,实验结果如表所示。
序号 | A:0.2mol·L-1NaCl | B:0.1mol·L-1FeSO4 | 电流计读数 |
实验1 | pH=1 | pH=5 | 8.4 |
实验2 | pH=1 | pH=1 | 6.5 |
实验3 | pH=6 | pH=5 | 7.8 |
实验4 | pH=6 | pH=1 | 5.5 |
(资料 2)原电池装置中,其它条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原 电池的电流越大。
(资料 3)常温下,0.1mol/L pH=1 的 FeSO4 溶液比 pH=5 的 FeSO4 溶液稳定性更好。 根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U 型管中左池的电极反应式____________。
②对比实验 1 和 2(或 3 和 4) ,在一定 pH 范围内,可得出的结论为____________。
③对比实验____________和____________,还可得出在一定pH 范围内溶液酸碱性变化对 O2 氧化性强弱的影响因素。
④ 对(资料 3)实验事实的解释为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于价电子排布式为![]() 的原子的描述正确的是( )
的原子的描述正确的是( )
A.该原子核外有三种形状不同的电子云
B.该原子核外电子共有16种不同的运动状态
C.该原子形成的单质可与H2反应生成常温下为液态的化合物
D.基态该原子的轨道表示式为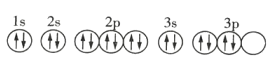
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外仅有一个非空原子轨道,也是宇宙中最丰富的元素;B元素原子核外p电子数比s电子数少1;C为金属元素且原子核外p电子数和s电子数相等;D元素的原子核外所有p轨道为全充满或半充满状态。
(1)写出四种元素的元素符号:A__________ ,B__________,C__________ ,D__________ 。
(2)写出C、D两种元素基态原子的轨道表示式:
C ________________________________
D ___________________________
(3)写出B、C两种元素的单质在一定条件下反应的化学方程式:________________________。
(4)B元素的单质的电子式为_____________,其最简单氢化物的电子式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿斯巴甜是一种具有清爽甜味的有机化合物,结构简式如图所示。下列说法不正确的是( )
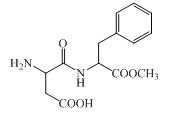
A.分子式为C14H18N2O5
B.不存在顺反异构
C.能发生取代和消去反应
D.1 mol阿斯巴甜完全水解最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】符合分子式“C6H6”的多种可能结构如图所示,下列说法正确的是

A. 1~5对应的结构中能使溴的四氯化碳溶液褪色的有4个
B. 1~5对应的结构中一氯取代物只有1种的有3个
C. 1~5对应的结构中所有原子均可能处于同一平面的有1个
D. 1~5对应的结构均能与氢气在一定条件下发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)分子式为 C2H6O 的有机物,有两种同分异构体,乙醇(CH3CH2OH)、甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是 (_________)
A.红外光谱 B. 1H 核磁共振谱 C.质谱法 D.与钠反应
(2)有机物 A 只含有 C、H、O 三种元素,常用作有机合成的中间体。16.8g 该有机物在足 量 O2中充分燃烧生成 44.0gCO2 和 14.4gH2O,质谱图表明其相对分子质量为 84,分析其红 外光谱图可知 A 分子中含有 O-H 键和位于端点处的 C C 键,核磁共振氢谱上有三组峰, 峰面积之比为6:1:1。A的结构简式是______________________。
(3)已知乙烯分子是平面结构, 1,2-二氯乙烯可形成![]() 和
和![]() 两种不 同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_________)
两种不 同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_________)
A.1-丙烯 B.4-辛烯 C.1-丁烯 D.2-甲基-1-丙烯
(4)请写出 C(CH3)3Br与NaOH溶液、乙醇混合加热的反应方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,两体积均为1 L的容器中发生反应:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。容器中起始各物质的物质的量如下表所示,两容器中c(H2)随时间t的变化如下图所示。
CH3OH(g) ΔH。容器中起始各物质的物质的量如下表所示,两容器中c(H2)随时间t的变化如下图所示。
容器 | 温度 | CO | H2 | CH3OH |
Ⅰ | T1℃ | a mol | 2 mol | 0 mol |
Ⅱ | T1℃ | 0.5 mol | 1 mol | 0 mol |

下列说法正确的是
A.0~5 min时,容器Ⅰ中v(CO)=0.1 mol·L-1·min-1
B.a>1
C.若容器Ⅱ温度改变为T2(T2>T1)时,平衡常数K=1,则ΔH<0
D.T1℃时,若向容器Ⅰ中充入CO、H2、CH3OH各1 mol,反应将向逆反应方向进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com