
【题目】下列叙述正确的是( )
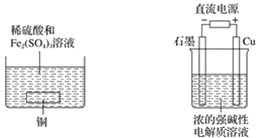
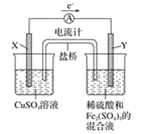
图1 图2 图3
A. 如图 1 所示,若铜中含有杂质银,可形成原电池,且铜作负极
B. 如图 2 所示,当有 0.1 mol 电子转移时,有 0.1 mol Cu2O 生成
C. 基于绿色化学理念设计的制取 Cu2O 的电解池如图 2 所示,铜电极发生还原反应
D. 若图 3 所示的装置中发生 Cu+2Fe3+===Cu2++2Fe2+的反应,则 X 极是负极,Y 极的材料可 以是铜
【答案】A
【解析】
A项、若铜中含有杂质银,铜能硫酸铁溶液发生氧化还原反应,能构成原电池,铜做原电池的负极,银故原电池的正极,故A正确;
B项、该装置为电解池,与电源正极相连的铜电极为阳极,铜失电子发生氧化反应生成氧化亚铜,当有0.1mol电子转移时,有0.05mol Cu2O生成,故B错误;
C项、该装置为电解池,与电源正极相连的铜电极为阳极,铜失电子发生氧化反应生成氧化亚铜,故C错误;
D项、该装置为原电池,由电子的移动方向可知,X极是原电池的负极,Y极为原电池的正极,由方程式Cu+2Fe3+=Cu2++2Fe2+可知,Cu为负极,Y极应为活泼性小于铜的金属或者非金属,不可以是铜,故D错误。
故选A。


科目:高中化学 来源: 题型:
【题目】化学家合成了一种新化合物(如图所示),其中A、B、C、D为原子序数依次增大的短周期主族元素,B与C在同一主族,C与D在同一周期。下列有关说法正确的是
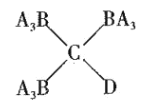
A.熔点:B的氧化物>C的氧化物
B.工业上由单质B可以制得单质C
C.氧化物对应水化物的酸性:D>B>C
D.A与B形成的化合物中只含有极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给某潜水器提供动力的电池如图所示。下列有关说法正确的是( )
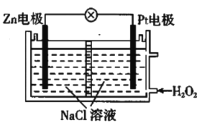
A.Zn极发生了还原反应
B.电池中的Na+向Zn电极移动
C.Pt电极反应式为H2O2+2e-=2OH-
D.电子从Zn电极沿导线流向Pt电极,再经溶液回到Zn电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组做了如下实验探究海带中碘元素的存在形式,探究过程如图:

(1)操作I为灼烧,则灼烧时应该用___(仪器名称)盛装海带,操作II为___;
(2)水浸时通常要将悬浊液煮沸2-3min,目的是___。
(3)操作III,是同学们对溶液A中碘元素的存在形式进行的探究实验。
推测:①以IO![]() 形式存在②以I-形式存在
形式存在②以I-形式存在
查阅资料:IO![]() 具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
限选试剂:3%H2O2溶液、KSCN溶液、FeC12溶液、稀硫酸
序号 | 实验操作 | 实验现象 | 结论 |
① | 取少量稀释后的溶液A加入淀粉后再 用硫酸酸化,分装于试管I、II | 无现象 | |
② | 往试管I中加入FeC12溶液,然后加入2滴KSCN溶液并振荡; | ___ | 证明不是以IO |
③ | 往试管II中加入___; | ____ | 证明以I-形式存在 |
(4)取20mL稀释后溶液A于锥形瓶,滴加0.01mo1/LKMnO4溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B;已知在酸性条件下,MnO![]() 的还原产物为Mn2+,写出离子方程式___。
的还原产物为Mn2+,写出离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
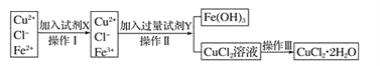
请参照下表给出的数据填空。

(1)操作I加入X的目的是___________________________ 。
(2)下列物质都可以作为X,适合本实验的X物质可以是_________(填字母)。
A KMnO4 B NaClO C H2O2 D Cl2
(3)操作II的Y试剂为____________(填化学式),并调节溶液的pH在______范围。
(4)实验室在配制CuCl2溶液时需加入少许_________(填物质名称),理由是(文字叙述并用有关离子方程式表示)__________________________________________。
(5)若将CuCl2溶液蒸干灼烧,得到的固体是_________________(填化学式);若要得无水CuCl2,请简述操作方法______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)苯、四氯化碳、乙醇、汽油是常见的有机溶剂,能与水互溶的是________;不溶于水,且密度比水小的是________。
(2)一瓶无色气体,可能含有CH4和CH2=CH2或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐退去,瓶壁有少量无色油状小液滴。
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确?________(填“正确”或“不正确”),理由是______________________。
②上述实验可能涉及的反应类型有_________________________。
(3)含有![]() 的化合物与CH2=CH2一样,在一定条件下可聚合成高分子化合物。
的化合物与CH2=CH2一样,在一定条件下可聚合成高分子化合物。
①广泛用作农用薄膜的聚氯乙烯塑料,是由![]() 聚合而成的,其化学方程式是________________________。
聚合而成的,其化学方程式是________________________。
②电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯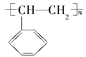 ,它是由________(写结构简式)聚合而成的。
,它是由________(写结构简式)聚合而成的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下铁可以和 CO2 发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 CO2 气体,反应过程中 CO2 气体和 CO 气体的浓度与时间的关系如图所示:

(1)t1 时,正、逆反应速率的大小关系为 v 正_____v 逆(填“>”“<”或“=”)。
(2)4 min 内,CO 的平均反应速率 v(CO)=_____。
(3)下列条件的改变能减慢其反应速率的是_____(填序号,下同)。
①降低温度
②减少铁粉的质量
③保持压强不变,充入 He 使容器的体积增大
④保持容积不变,充入 He 使体系压强增大
(4)下列描述能说明上述反应已达平衡状态的是_____。
①v(CO2)=v(CO)
②单位时间内生成 n mol CO2 的同时生成 n mol CO
③容器中气体压强不随时间变化而变化
④容器中气体的平均相对分子质量不随时间变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面列出了几组物质,请将物质的合适组号填写在空格上。
A.金刚石与石墨;B.淀粉与纤维素;C.氕与氘;D.甲烷与戊烷;E.葡萄糖与果糖F.![]() 与
与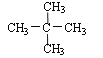 ;G.
;G.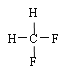 与
与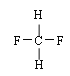 。
。
(1)同位素________________;
(2)同素异形体_______________;
(3)同系物_______________;
(4)同分异构体________________;
(5)同一物质________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用以下三种途径来制取相同质量的硝酸铜:①铜跟浓硝酸反应,②铜跟稀硝酸反应,③铜跟氧气反应生成氧化铜,氧化铜再跟稀硝酸反应。以下叙述正确的是( )
A.三种途径所消耗的铜的物质的量不相等
B.三种途径所消耗的硝酸的物质的量相等
C.所消耗铜的物质的量:途径③>途径①>途径②
D.所消耗硝酸的物质的量:途径①>途径②>途径③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com